题目内容
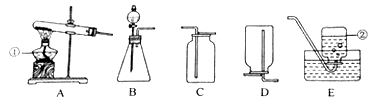
【题目】利用下图装置进行气体的制取实验,请回答下列问题:
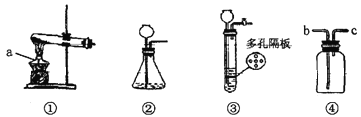
(1)写出标号a仪器的名称:________________。
(2)用氯酸钾制取氧气的化学方程式____________________,选择④装置收集氧气,气体从_______(填字母)端进入。若改用排水法收集,实验结束后先撤导气管后熄灭酒精灯,目的是防止___________________________。
(3)实验室用大理石和_________________(填写药品名称)反应制取二氧化碳。与②相比,③作为发生装置的优点是____________________,在装置④中盛放___________可用于干燥二氧化碳气体。
【答案】(1)酒精灯(2)2KC1O3![]() 2KC1+3O2↑; b ;水倒流入试管,使试管炸裂
2KC1+3O2↑; b ;水倒流入试管,使试管炸裂
(3)稀盐酸(写化学式不给分);可以控制反应的开始和停止(或可以控制反应的发生和结束;随开随用,随关随停);浓硫酸(浓H2SO4)
【解析】(1)由图可知,a是酒精灯;(2)在加热和二氧化锰的催化作用下,氯酸钾分解生成氯化钾和氧气,反应的化学方程式表示为2KC1O3![]() 2KC1+3O2↑;氧气的密度比空气大,会先聚集在集气瓶的上部,故氧气应从b端通入;用排水法收集氧气时,反应结束后要先撤除导气管,最后熄灭酒精灯,目的是防止水水倒流入试管,使试管炸裂;(3)实验室用石灰石或大理石和稀盐酸反应制取二氧化碳;装置③中可将石灰石放在隔板上,然后从长颈漏斗中加入稀盐酸,药品接触,反应发生,不需要反应时,用止水夹夹住橡皮管,稀盐酸进行长颈漏斗中,石灰石和稀盐酸分离,反应停止,故装置③的优点是可控制反应的发生与停止;可用浓硫酸作为干燥剂来干燥二氧化碳。
2KC1+3O2↑;氧气的密度比空气大,会先聚集在集气瓶的上部,故氧气应从b端通入;用排水法收集氧气时,反应结束后要先撤除导气管,最后熄灭酒精灯,目的是防止水水倒流入试管,使试管炸裂;(3)实验室用石灰石或大理石和稀盐酸反应制取二氧化碳;装置③中可将石灰石放在隔板上,然后从长颈漏斗中加入稀盐酸,药品接触,反应发生,不需要反应时,用止水夹夹住橡皮管,稀盐酸进行长颈漏斗中,石灰石和稀盐酸分离,反应停止,故装置③的优点是可控制反应的发生与停止;可用浓硫酸作为干燥剂来干燥二氧化碳。

【题目】实验探究一:课本第二单元课后作业中有“寻找新的催化剂” 的探究内容,实验中学探究小组据此设计了如下探究方案。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
实验步骤 | 实验现象 | 实验结论及解释 |
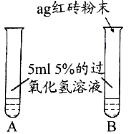
Ⅰ. | A中无明显现象, B中产生大量能使带火星木条复燃的气体 | ① 产生的气体是______ ② 红砖粉末能改变过氧化氢分解速率 |
Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag | 红砖粉末的_____在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
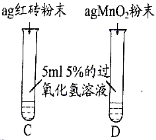
Ⅲ. | 两试管中均产生气泡且______ | 红砖粉末的催化效果没有二氧化锰粉末好 |
【拓展应用】
己知CuSO4也可作为过氧化氢分解的催化剂。向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气_____g。
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究。
【提出猜想】1.未变质 2.部分变质 3.完全变质
【查阅资料】KOH与NaOH性质类似,也能与CO2反应而变质。写出KOH变质的化学方程式为_____。
【设计实验】
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想_____不成立。
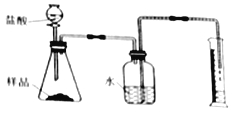
(2)准确称取一定质量的固体样品,放在右图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由_________。
(3)请你另外设计一个方案,进一步探究变质情况
实验步骤 | 实验现象 | 实验结论 |
猜想2成立 |