题目内容
【题目】在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
物质 | X | Y | Z | Q |
反应前的质量/g | 35 | 8 | 2 | 5 |
反应后的质量/g | 待测 | 1 | 42 | 3 |
下列说法正确的是 ( )
A.该反应属于化合反应B.该反应中X与Z是生成物
C.该反应中X与Y发生变化的质量比为35:8D.该反应中生成42gZ物质
【答案】A
【解析】
根据质量守恒定律,反应前物质的总质量等于反应后物质的总质量,则![]() ,
,![]() 。
。
A、根据质量守恒定律,反应前物质的总质量等于反应后物质的总质量,则![]() ,
,![]() ,反应前后,X、Y、Q的质量减少,为反应物,Z的质量增加,为生成物,该反应属于化合反应,故A正确;
,反应前后,X、Y、Q的质量减少,为反应物,Z的质量增加,为生成物,该反应属于化合反应,故A正确;
B、反应前后,X的质量减少,为反应物,Z的质量增加,为生成物,故B不正确;
C、该反应中X与Y发生变化的质量比为![]() ,故C不正确;
,故C不正确;
D、该反应中生成![]() Z物质,故D不正确。故选A。
Z物质,故D不正确。故选A。

 名校课堂系列答案
名校课堂系列答案【题目】某班同学按下图所示的实验探究质量守恒定律。
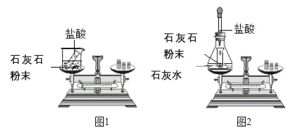
(1)同学们先按图1的方式实验,该实验中,大家进行了两次称量,有四个小组得到下列数据,其中有问题的两组数据是_____(填字母)。
A | B | C | D | |
盐酸加入CaCO3粉末前称量/g | 85.3 | 82.8 | 84.8 | 86.5 |
盐酸加入CaCO3粉末后称量/g | 85.3 | 80.6 | 83.2 | 87.8 |
(2)同学们又按照图2的方式实验,当天平平衡后,挤压胶头滴管逐滴滴入盐酸,最终天平的状态是_____(填字母)。
A 左盘高
B 右盘高
C 保持平衡
(3)该实验中通过化学反应新生成的物质有_____、_____(填字母)。
A HCl
B CO2
C CaCO3
D NaOH
【题目】计算:某同学为了研究实验室中用某氯酸钾样品制氧气的有关问题,他将5g该样品与1g二氧化锰混合,加热该混合物(假设杂质不参加反应),在不同时间测得有关数据如下表:
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量/g | 5.04 | 4.08 | ||
生成氧气的质量/g | 1.84 | 1.92 |
(1)加热t3时间后氯酸钾是否已经完全反应?________(填“是”或“否”),此时二氧化锰的质量为______________g。
(2)该样品中氯酸钾的质量为_______________?
【题目】现有氧化铜和铜的混合物,对其成分组成进行分析。取20g此样品,向其中分三次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
第一次 | 第二次 | 第三次 | |
加入稀硫酸的质量/g | 80 | 80 | 80 |
充分反应后剩余固体质量/g | 12 | 8 | m |
试回答下列问题:
(1)上述表格中m的值为______。
(2)所用稀硫酸的溶质质量分数为___?
(3)充分反应后所得硫酸铜溶液的溶质质量分数为____?(结果保留0.1%)