题目内容
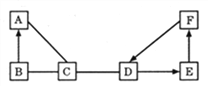
【题目】天启同学为了探究碳及其氧化物的某些性质,用如图装置进行实验:
(提示:B装置目的是为了除去杂质HCl气体)
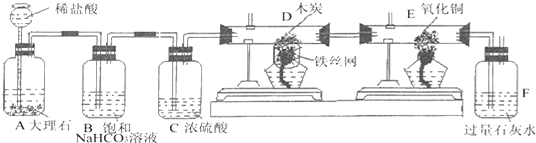
请根据如图图回答下列问题:
(1)写出下列装置中发生的化学反应方程式:E装置_________,F装置_________.
(2)D装置中发生的化学反应的基本反应类型_______,C装置中的作用是____.
(3)该装置的不足之处是______.
【答案】 CO+CuO![]() Cu+CO2 ;. CO2 + Ca(OH)2 == CaCO3 ↓+ H2O 化合反应 干燥二氧化碳 没有尾气处理装置
Cu+CO2 ;. CO2 + Ca(OH)2 == CaCO3 ↓+ H2O 化合反应 干燥二氧化碳 没有尾气处理装置
【解析】(1)碳酸钙和稀盐酸反应,生成二氧化碳,氯化钙和水,化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑;D中碳与二氧化碳反应能生成一氧化碳,反应方程式为:CO2+C ![]() 2CO;E中一氧化碳能与氧化铜反应生成铜和二氧化碳,化学方程式CO+CuO
2CO;E中一氧化碳能与氧化铜反应生成铜和二氧化碳,化学方程式CO+CuO![]() Cu+CO2; F中二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应方程式为:CO2 + Ca(OH)2 == CaCO3 ↓+ H2O;(2)D中碳与二氧化碳反应能生成一氧化碳,是由两种物质生成一种物质的化合反应;C中浓硫酸的作用是干燥二氧化碳;(3)一氧化碳具有毒性,需要进行尾气处理,以防污染空气。
Cu+CO2; F中二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应方程式为:CO2 + Ca(OH)2 == CaCO3 ↓+ H2O;(2)D中碳与二氧化碳反应能生成一氧化碳,是由两种物质生成一种物质的化合反应;C中浓硫酸的作用是干燥二氧化碳;(3)一氧化碳具有毒性,需要进行尾气处理,以防污染空气。

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组的同学,为了比较金属R与铁、铜的金属活动性强弱,进行如下探究活动:
[查阅资料]铁的活动性比铜强.
[进行猜想]对三种金属的活动性顺序做出如下猜想:
猜想一:R>Fe>Cu; 猜想二:_______________; 猜想三:Fe>Cu>R
[收集证据]为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究.
主要操作 | 主要现象 | 实验结论 | |
甲 | 将打磨好的R丝插入盛有硫酸铜溶液的试管中 | ______________ | 猜想一 正确 |
乙 | 将粗细相同打磨好的R丝、铁丝,分别插入体积和溶质质量分数都相同的稀盐酸中 | R丝表面产生气泡速率比铁丝表面产生气泡速率___(填“快”或“慢”) | |
丙 | 将粗细相同打磨好的R丝、铁丝,分别在空气中点燃 | R丝在空气中剧烈燃烧,铁丝在 空气中______ |
写出铁丝在氧气中燃烧的化学方程式__________________________________
[交流反思]三位同学交流讨论后认为,比较金属活动性强弱的方法有多种.
[归纳总结]他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与酸溶液是否反应或反应的剧烈程度;
(3)金属与_____是否反应.
【题目】下列实验方法一定能达到实验目的的是
选项 | 实验目的 | 实验方法 |
A | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
B | 鉴别 | 分别点燃,在火焰上方罩一干冷烧杯 |
C | 鉴别石灰水和 | 加入适量的稀盐酸 |
D | 比较Zn、Cu、Ag的金属活动性 | 将Zn和Ag分别放入 |