��Ŀ����
����Ŀ������ij��ѧС���ͬѧ��ѧϰ���кͷ�Ӧ������ʵ���������ǽ�һ����������������Һ��ϡ�����ϣ� 
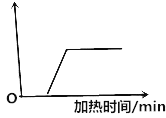
��1����ͼ1��ʾ���䷴Ӧ�Ļ�ѧ����ʽΪ��ͬѧ�Ƿ��ָ÷�Ӧû�����Ե�������������ʵ��̽����
��2�����������1�������֤�÷�Ӧ�Ѿ�������
������ʵ�顿ͬѧ�Ƿֱ�ȡͼ1Bͼ����Һ������������ʵ�飬�����ͼ��ʾ��
����Ӧ���ۡ�����Ϊ����ʵ������֤��Ӧ�Ѿ���������ʵ�� �� ��ѡ��������һʵ����۽Ƕȷ�������ȷ���������� ��
��3�����������2��ͼ1Bͼ��Һ�����ʵijɷ�����Щ��
������ʵ�顿
ʵ����� | ʵ������ | ���� |
ȡBͼ�е�������Һ���Թ��м��� | �۲쵽 | Bͼ����Һ��������Na2SO4��H2SO4 |
��˼����ͬѧ����Ϊ����һ�ֲ�ͬ�����Լ� �� Ҳ�ܴﵽ��ͬ��Ŀ�ģ�
��4������չ���졿��Cͼ�Թ��е����ʾ��ã��ϲ���Һ��һ�����е������� ��
���𰸡�
��1��2NaOH+H2SO4=Na2SO4+2H2O
��2������ʵ��һ��![]()
![]() ���μӷ�Ӧ����ʵ����п�֤��
���μӷ�Ӧ����ʵ����п�֤��![]() ȫ����Ӧ��
ȫ����Ӧ��
��3����ɫʯ����Һ����ɫʯ���죻���ۻ�Na2CO3
��4��NaCl��HCl
���������⣺�������������ᷢ���кͷ�Ӧ���������ƺ�ˮ�����2NaOH+H2SO4=Na2SO4+2H2O��
����˼���ۡ�����������Һ�Լ��ԣ���ʹ��ɫ�ķ�̪��Һ���ɫ�����Ǽ���ϡ�������ɫ��˵�����е��������Ʋ����˷�Ӧ��ʵ��һ��֤�����߷����˷�Ӧ����Ϊ���е����������û�в��뷴Ӧ���μ��Ȼ�����Һһ���������ɫ������ʵ�����֤������Ϊ��̪��Һ�������ɫ��˵��������������ȫ�����˷�Ӧ���������ʵ��һ�� ![]() ���μӷ�Ӧ����ʵ����п�֤��
���μӷ�Ӧ����ʵ����п�֤��![]() ȫ����Ӧ����
ȫ����Ӧ����
������ʵ�顿Ҫ�����Ƿ�������Ĵ��ڣ��ɼ�����ɫ��ʯ����Һ�����飬����Һ�еμ���ɫ��ʯ����Һ������˺�ɫ����֤���������ᣬҲ�ɼ������ۻ�̼���Ʒ�ĩ���������ݲ�������֤��������Ĵ��ڣ������ɫʯ����Һ����ɫʯ���죻���ۻ�Na2CO3���������ɣ�
����չ���졿
�������������Ʒ�Ӧ�����������ƺ�ˮ�������еμ��Ȼ�����Һ�����������ᱵ��ɫ�������Ȼ��ƣ���Ϊ��������������������Ȼ�����Һ��Ӧ�������ᱵ��ɫ���������������Һ�д����Ȼ��ƺ��Ȼ����������ʣ����NaCl��HCl��
�����㾫����ͨ����������кͷ�Ӧ����Ӧ�ú���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�������кͷ�Ӧ����������������κ�ˮ�ķ�Ӧ��ע�⣺a����ƽ b������ c�����ż����Խ����⣮

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�