题目内容
CO和CO2两种物质中,相同的是
- A.碳的质量分数
- B.氧的质量分数
- C.原子个数比
- D.元素种类
D
分析:根据CO和CO2的元素组成,分子构成和性质进行判断,二者的都是由碳氧元素组成的,每个分子中所含原子个数不同,元素的质量比就不同,根据元素的质量分数= ×100%,判断元素质量分数是否相同.
×100%,判断元素质量分数是否相同.
解答:A、一氧化碳中碳元素的质量分数= ×100%=
×100%=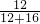 ×100%=≈43%,二氧化碳中碳元素的质量分数=
×100%=≈43%,二氧化碳中碳元素的质量分数= ×100%=
×100%=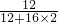 ×100%≈27%,碳元素质量分数不同,故C错误;
×100%≈27%,碳元素质量分数不同,故C错误;
B、一氧化碳中氧元素的质量分数= ×100%=
×100%= ×100%≈57%,二氧化碳中氧元素的质量分数=
×100%≈57%,二氧化碳中氧元素的质量分数= ×100%=
×100%=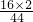 ×100%≈72%,氧元素质量分数不同,故B错误;
×100%≈72%,氧元素质量分数不同,故B错误;
C、一个一氧化碳分子中含有两个原子,一个二氧化碳分子中含有三个原子,原子个数比为2:3,故C错误;
D、CO和CO2都是由碳氧元素组成的,元素种类相同,故D正确.
故选D.
点评:本题考查的是学生对化学式的认知情况,有利于学生对这部分知识的整体认知.
分析:根据CO和CO2的元素组成,分子构成和性质进行判断,二者的都是由碳氧元素组成的,每个分子中所含原子个数不同,元素的质量比就不同,根据元素的质量分数=
 ×100%,判断元素质量分数是否相同.
×100%,判断元素质量分数是否相同.解答:A、一氧化碳中碳元素的质量分数=
 ×100%=
×100%=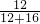 ×100%=≈43%,二氧化碳中碳元素的质量分数=
×100%=≈43%,二氧化碳中碳元素的质量分数= ×100%=
×100%=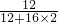 ×100%≈27%,碳元素质量分数不同,故C错误;
×100%≈27%,碳元素质量分数不同,故C错误;B、一氧化碳中氧元素的质量分数=
 ×100%=
×100%= ×100%≈57%,二氧化碳中氧元素的质量分数=
×100%≈57%,二氧化碳中氧元素的质量分数= ×100%=
×100%=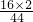 ×100%≈72%,氧元素质量分数不同,故B错误;
×100%≈72%,氧元素质量分数不同,故B错误;C、一个一氧化碳分子中含有两个原子,一个二氧化碳分子中含有三个原子,原子个数比为2:3,故C错误;
D、CO和CO2都是由碳氧元素组成的,元素种类相同,故D正确.
故选D.
点评:本题考查的是学生对化学式的认知情况,有利于学生对这部分知识的整体认知.

练习册系列答案
相关题目
 北京奥运火炬“祥云”的火种采集工作将于2008年3月25日在希腊奥林匹亚进行.届时,将用采集的火种点燃奥运火炬.
北京奥运火炬“祥云”的火种采集工作将于2008年3月25日在希腊奥林匹亚进行.届时,将用采集的火种点燃奥运火炬.