题目内容
甲、乙、丙同学分别取10克氯酸钾与二氧化锰的混合物,加热不同时间来制取氧气.根据以下信息回答:
| 甲(加热2分钟) | 乙(加热4分钟) | 丙(加热6分钟) | |
| 残留固体质量 | 8.62克 | 7.12克 | 7.12克 |
(3)原混合物中二氧化锰的质量分数.
解:(1)氯酸钾分解的化学方程式为:2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
(2)完全反应后,生成氧气的质量为:10g-7.12g=2.88g;
(3)设氯酸钾的质量为X,
2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
245 96
X 2.88g
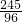 =
=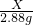
X=7.35g,
二氧化锰的质量为:10g-7.35g=2.65g,
二氧化锰的质量分数为: ×100%=26.5%;
×100%=26.5%;
答:生成氧气的质量是2.88g,二氧化锰的质量分数是26.5%.
分析:(1)氯酸钾在二氧化锰的催化作用下受热分解生成氯化钾和氧气;
(2)根据质量差可以计算生成氧气的质量;
(3)根据化学方程式可以计算氯酸钾的质量,进一步可以计算二氧化锰的质量.
点评:本题主要考查计算能力,特别是差量法的运用能够使计算更加简单.
 2KCl+3O2↑;
2KCl+3O2↑;(2)完全反应后,生成氧气的质量为:10g-7.12g=2.88g;
(3)设氯酸钾的质量为X,
2KClO3
 2KCl+3O2↑;
2KCl+3O2↑;245 96
X 2.88g
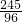 =
=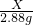
X=7.35g,
二氧化锰的质量为:10g-7.35g=2.65g,
二氧化锰的质量分数为:
 ×100%=26.5%;
×100%=26.5%;答:生成氧气的质量是2.88g,二氧化锰的质量分数是26.5%.
分析:(1)氯酸钾在二氧化锰的催化作用下受热分解生成氯化钾和氧气;
(2)根据质量差可以计算生成氧气的质量;
(3)根据化学方程式可以计算氯酸钾的质量,进一步可以计算二氧化锰的质量.
点评:本题主要考查计算能力,特别是差量法的运用能够使计算更加简单.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目