题目内容
【题目】传统干电池在日常生活中有多方面的应用,如图显示的是干电池的内部构造,请回答下列问题: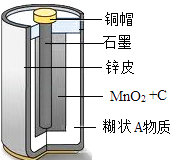
(1)干电池是把能转化为电能,写出干电池正极材料主要成分的化学式:;
(2)上述材料中属于金属材料的是(写一种);
(3)取干电池内的填充物溶于水,过滤,滤渣成分是MnO2和C,为了得到比较纯净的MnO2 , 可采用的简单方法是 .
(4)MnO2在实验室利用过氧化氢溶液制取O2中起的是作用.
(5)糊状A物质的成分之一是氯化铵,请你写出该物质中阳离子的符号: .
【答案】
(1)化学,C
(2)铜或锌
(3)在空气中充分灼烧
(4)催化
(5)NH4+
【解析】(1)干电池放电时是通过化学变化产生能量,把化学能转化为电能.干电池正极是碳棒,材料主要成分的化学式:C;
(2)金属材料包括纯金属和合金,干电池中铜帽、锌皮都属于金属材料;
(3)由于碳可以与空气中的氧气反应生成二氧化碳,而二氧化锰不可以,所以从MnO2和C中得到比较纯净的MnO2,可以在空气中充分灼烧;
(4)实验室制氧气常用MnO2作催化剂;
(5)氯化铵是由铵根离子和氯离子构成的,其中的阳离子是铵根离子,故填:NH4+.
所以答案是:(1)化学;C(2)铜或锌;(3)在空气中充分灼烧;(4)催化;(5)NH4+.
【考点精析】通过灵活运用催化剂的特点与催化作用和碳的化学性质,掌握催化剂(触媒):在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质.(一变两不变)催化剂在化学反应中所起的作用叫催化作用;各种单质碳的化学性质却完全相同;1、常温下的稳定性强2、可燃性:完全燃烧(氧气充足),生成CO2;不完全燃烧 (氧气不充足),生成CO;3、还原性:应用:冶金工业;现象:黑色粉末逐渐变成光亮红色,石灰水变浑浊即可以解答此题.

 名校课堂系列答案
名校课堂系列答案【题目】为了防止食品腐败,在许多食品包装盒中都有一包黑色粉末。这种粉末是一种除氧剂。该粉末没有失效时呈黑色,失效后带有红棕色。
为了确定该粉末的成分,小明做出了以下的【猜想】:
猜想1:该粉末是木炭粉 猜想2:该粉末是铁粉 猜想3:该粉末是木炭粉和铁粉的混合物
小明取没有失效的该粉末,分别用不同的方法进行如下实验,填写表中空格。
试验操作 | 试验现象 | 猜想是否成立 | |
实验1 | 加入足量的硫酸铜溶液 | __________________ | 猜想1:不成立 |
实验2 | 加入足量的_________ | __________________ | 猜想2:成立 |
实验3 | 用磁铁吸引 | 粉末被全部吸引 | 猜想3:__________ |
【交流与反思】
(1)根据失效后的颜色判断,该粉末失效的原因是_______________________,变质后得到的红棕色粉末的主要成分是_____________(填物质的化学式)。
(2)采用什么实验方法可以使失效的粉末“再生”?(用化学方程式表示)_____________。
【题目】小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.具体是什么物质无法辨认.老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或是碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,认为该溶液不可能是氢氧化钙,理由是
(2)小亮取少量样品于试管中,滴加试液.试液变红色,该溶液不可能是(填写化学式),理由是 .
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请一起参与,并填写下列实验报告.
【设计实验方案】方案甲:选择氯化钙溶液来确定该溶液的成份;
方案乙:选择稀盐酸来确定该溶液的成份.
【进行实验】你愿意选择方案 (选填“甲”或“乙”)进行实验.
实验步骤 | 实验现象 | 实验结论 |
取少量溶液于试管中,滴加 | 该溶液是碳酸钠溶液. |
(4)【实验反思】(附加题)
①玉鹏同学认为还可以用一种不同于甲、乙类别的物质来确定,请你帮他完成(此题为附加题总分不超过60分),该物质可以为 .
实验步骤 | 实验现象 | 实验结论 |
取少量溶液于试管中,滴加该物质 | 该溶液是碳酸钠溶液. |
②小亮经过反思,向同学们提出如下建议,你认为合理的是 (填序号).
A.倾倒液体时应注意保护标签不被腐蚀
B.要有严谨的科学实验的态度
C.无法辨认的药品,直接倒掉,无需保留.