题目内容
(2004?汕头)有1包粉末,可能由C、CuO、Fe三种物质中的一种或几种组成.某同学为了探究它的成分,按如下步骤进行实验.(1)先对实验做了如下设想和分析.取少量粉末于烧杯中,向烧杯中加入过量的稀硫酸,则实验中可能出现的现象与对应结论如下表所示(表中未列完所有情况).请你完成下表.
| 烧杯中可能出现的现象 | 结 论 |
| ①______ | 只含C |
| ②______ | 含C、CuO |
| ③有黑色不溶物,有气泡逸出,溶液呈浅绿色 | ______ |
实验1:将此粉末敞口在空气中灼烧完全,待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置.烧杯中______(填“有”或“无”)不溶物,溶液呈______颜色.
实验2:将此粉末隔绝空气加热(若碳完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置.请回答:
①烧杯中______(填“有”或“无”)不溶物;
②若静置后溶液呈无色,则该溶液中溶质是______(写化学式);
③若静置后溶液呈蓝色,该实验过程中所发生反应的化学方程式为______ 2Cu+CO2↑
【答案】分析:(1)根据碳不与稀硫酸反应;氧化铜可以与稀硫酸反应,生成的铜离子在水溶液中显蓝色;铁可以与稀硫酸反应放出气体,且生成的亚铁盐的水溶液中显绿色;
(2)实验1:根据C会与氧气反应生成二氧化碳气体,氧化铜会与稀硫酸反应生成硫酸铜溶液;
实验2:碳单质具有还原性.可以将氧化铜还原为红色的铜,且铜不与稀硫酸反应.
解答:解:(1)①因为碳不与稀硫酸反应,可以观察的现象为:固体质量不减少,且溶液仍为无色;
②因为碳不与稀硫酸反应,但氧化铜可以与稀硫酸反应生成铜盐溶液,其水溶液为蓝色,所以观察到的现象为:有黑色不溶物,溶液由无色变为蓝色;
③因为黑色的碳不与稀硫酸反应,但Fe可以与稀硫酸反应生成氢气和亚铁盐,亚铁盐的水溶液为浅绿色;
(2)实验1:因为碳可以与氧气反应生成二氧化碳气体,所以将此粉末在空气中灼烧完全后,剩余的固体是氧化铜,它可以与稀硫酸反应,生成蓝色的硫酸铜溶液;
实验2:①因为碳单质具有还原性,可以将氧化铜还原为红色的铜,所以将此粉末隔绝空气加热后,剩余的固体是Cu,而Cu不与稀硫酸反应;
②若静置后溶液无色,则说明氧化铜被全部还原,则溶质为硫酸;
③若静置后溶液呈蓝色,则说明还存在着氧化铜,故发生的反应为:氧化铜与碳,及氧化铜和硫酸的反应;
故答案为:(1)
(2)实验1:无、蓝;
实验2:①有
②H2SO4
③2CuO+C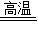 2Cu+CO2↑、CuO+H2SO4=CuSO4+H2O
2Cu+CO2↑、CuO+H2SO4=CuSO4+H2O
点评:熟练掌握常见物质的化学性质,知道碳具有还原性可以使氧化铜被还原,掌握常见离子的颜色,如:铜离子显蓝色,亚铁离子显浅绿色等.
(2)实验1:根据C会与氧气反应生成二氧化碳气体,氧化铜会与稀硫酸反应生成硫酸铜溶液;
实验2:碳单质具有还原性.可以将氧化铜还原为红色的铜,且铜不与稀硫酸反应.
解答:解:(1)①因为碳不与稀硫酸反应,可以观察的现象为:固体质量不减少,且溶液仍为无色;
②因为碳不与稀硫酸反应,但氧化铜可以与稀硫酸反应生成铜盐溶液,其水溶液为蓝色,所以观察到的现象为:有黑色不溶物,溶液由无色变为蓝色;
③因为黑色的碳不与稀硫酸反应,但Fe可以与稀硫酸反应生成氢气和亚铁盐,亚铁盐的水溶液为浅绿色;
(2)实验1:因为碳可以与氧气反应生成二氧化碳气体,所以将此粉末在空气中灼烧完全后,剩余的固体是氧化铜,它可以与稀硫酸反应,生成蓝色的硫酸铜溶液;
实验2:①因为碳单质具有还原性,可以将氧化铜还原为红色的铜,所以将此粉末隔绝空气加热后,剩余的固体是Cu,而Cu不与稀硫酸反应;
②若静置后溶液无色,则说明氧化铜被全部还原,则溶质为硫酸;
③若静置后溶液呈蓝色,则说明还存在着氧化铜,故发生的反应为:氧化铜与碳,及氧化铜和硫酸的反应;
故答案为:(1)
| 烧杯中可能出现的现象 | 结 论 |
| ①有黑色不溶物,溶液呈无色 | 只含C |
| ②有黑色不溶物,溶液呈蓝色 | 含C、CuO |
| ③有黑色不溶物,有气泡逸出,溶液呈浅绿色 | 含C、Fe |
实验2:①有
②H2SO4
③2CuO+C
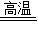 2Cu+CO2↑、CuO+H2SO4=CuSO4+H2O
2Cu+CO2↑、CuO+H2SO4=CuSO4+H2O点评:熟练掌握常见物质的化学性质,知道碳具有还原性可以使氧化铜被还原,掌握常见离子的颜色,如:铜离子显蓝色,亚铁离子显浅绿色等.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
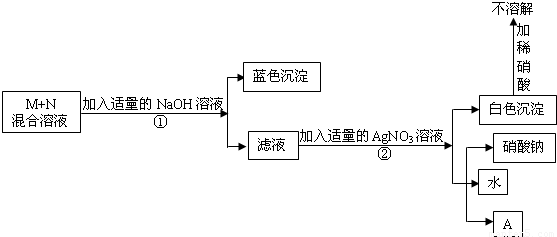
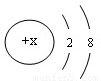 ,当x=12时,则该元素属于(填“金属”或“非金属”),该元素的原子核外有个电子层.
,当x=12时,则该元素属于(填“金属”或“非金属”),该元素的原子核外有个电子层.