题目内容
化学兴趣小组的同学在实验室测定某赤铁矿石中氧化铁的质量分数。取赤铁矿石样品10.0 g,加入稀盐酸109.5 g,恰好完全反应。过滤得到滤渣2.0 g(假设杂质既不溶于水也不与酸发生反应)。请计算:
(1)赤铁矿石中氧化铁的质量分数;
(2)反应后所得溶液中溶质的质量分数。
(计算结果精确到0.1%,写出必要的计算过程。可能用到得相对原子质量:H—1,C—12,O—16,Cl—35.5, Fe—56)
(1)赤铁矿石中氧化铁的质量分数 =" (10.0g-2.0g)/10.0g" ×100% = 80.0% (1分)
(2)设反应后溶液中溶质的质量为x。
Fe2O3 + 6HCl ="2" FeCl3 + 3H2O (2分)
160 2×162.5
8.0g x (1分)
160/8.0g=2×162.5/x
x = 16.25 g (1分)
溶液中溶质的质量分数=16.25 g/(109.5 g + 8.0g)×100% =13.8 % (1分)
答略。
(其它合理答案参考给分)
解析

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
 20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.
20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.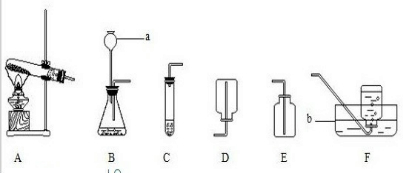
 (2012?太原)某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验:
(2012?太原)某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验: