题目内容
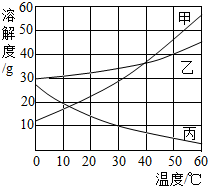 甲、乙、丙三种物质的溶解度曲线如图所示.根据溶解度曲线回答有关问题:
甲、乙、丙三种物质的溶解度曲线如图所示.根据溶解度曲线回答有关问题:(1)50℃时,物质乙的溶解度是
40g
40g
;(2)40℃时,在盛有50g水的三只烧杯中,分别加入a g甲、b g乙、c g丙,恰好得到甲、乙、丙三种物质饱和溶液时,所需三种物质的质量关系是
a=b>c
a=b>c
;(3)30℃时,将甲和丙两种物质的饱和溶液同时降温至0℃时,所得溶液中最小的溶质质量分数为
9.1
9.1
%(精确到0.1%);(4)从物质乙溶解度曲线上可以得到有关信息,你获取的两点信息是:
①
乙在0--60℃时,不同温度下的溶解度
乙在0--60℃时,不同温度下的溶解度
;②
随着温度的升高,物质乙的溶解度逐渐增加(合理均可)
随着温度的升高,物质乙的溶解度逐渐增加(合理均可)
.分析:(1)由溶解度曲线可知某温度下物质的溶解度;
(2)据该温度下三种物质的溶解度大小分析解答;
(3)据甲、丙的溶解度随温度变化情况及溶质的质量分数计算方法分析判断;
(4)据溶解度曲线可知不同温度下物质的溶解度,物质的溶解度随温度变化情况等.
(2)据该温度下三种物质的溶解度大小分析解答;
(3)据甲、丙的溶解度随温度变化情况及溶质的质量分数计算方法分析判断;
(4)据溶解度曲线可知不同温度下物质的溶解度,物质的溶解度随温度变化情况等.
解答:解:(1)50℃时,物质乙的溶解度是40g;
(2)40℃时甲、乙、丙的溶解度关系是甲=乙>丙,所以在盛有50g水的三只烧杯中,分别加入a g甲、b g乙、c g丙,恰好得到甲、乙、丙三种物质饱和溶液时,所需三种物质的质量关系是a=b>c;
(3)甲的溶解度随温度的降低而减小,丙的溶解度随温度的降低而增大,所以30℃时,将甲和丙两种物质的饱和溶液同时降温至0℃时,甲析出晶体,丙变为不饱和溶液,溶质的质量分数与降温前相等,据饱和溶液中溶质的质量分数的计算式
×100%可知:溶解度大则饱和溶液中 溶质的质量分数大,而0℃时甲的溶解度大于30℃时丙的溶解度,故所得溶液中最小的是丙,溶质质量分数为
≈9.%;
(4)由物质乙溶解度曲线可知乙在0--60℃时,不同温度下的溶解度,随着温度的升高,物质乙的溶解度逐渐增加,0℃时乙的溶解度小于甲的溶解度等;
故答案为:(1)40 g; (2)a=b>c; (3)9.1;
(4)乙在0--60℃时,不同温度下的溶解度; 随着温度的升高,物质乙的溶解度逐渐增加 (合理均可).
(2)40℃时甲、乙、丙的溶解度关系是甲=乙>丙,所以在盛有50g水的三只烧杯中,分别加入a g甲、b g乙、c g丙,恰好得到甲、乙、丙三种物质饱和溶液时,所需三种物质的质量关系是a=b>c;
(3)甲的溶解度随温度的降低而减小,丙的溶解度随温度的降低而增大,所以30℃时,将甲和丙两种物质的饱和溶液同时降温至0℃时,甲析出晶体,丙变为不饱和溶液,溶质的质量分数与降温前相等,据饱和溶液中溶质的质量分数的计算式
| 溶解度 |
| 溶解度+100g |
| 10g |
| 110g |
(4)由物质乙溶解度曲线可知乙在0--60℃时,不同温度下的溶解度,随着温度的升高,物质乙的溶解度逐渐增加,0℃时乙的溶解度小于甲的溶解度等;
故答案为:(1)40 g; (2)a=b>c; (3)9.1;
(4)乙在0--60℃时,不同温度下的溶解度; 随着温度的升高,物质乙的溶解度逐渐增加 (合理均可).
点评:本题考查了学生对于溶解度曲线的认识和应用,及溶质的质量分数计算,了解相关知识才能正确分析解答.

练习册系列答案
相关题目
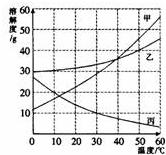 24、甲.乙.丙三种物质的溶解度曲线如图所示,据图回答:
24、甲.乙.丙三种物质的溶解度曲线如图所示,据图回答: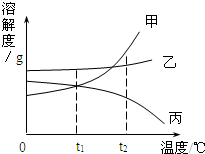 (2008?徐汇区一模)如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在),请根据右图回答:
(2008?徐汇区一模)如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在),请根据右图回答: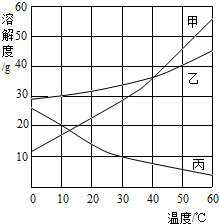 (2012?天津)甲、乙、丙三种物质的溶解度曲线如图所示.根据图中信息回答下列问题:
(2012?天津)甲、乙、丙三种物质的溶解度曲线如图所示.根据图中信息回答下列问题: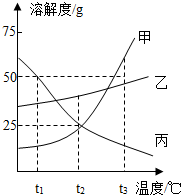 (2013?武汉)如图是甲、乙、丙三种物质的溶解度曲线.
(2013?武汉)如图是甲、乙、丙三种物质的溶解度曲线.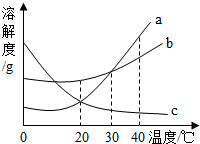 (2013?文昌一模)如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
(2013?文昌一模)如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题: