题目内容
【题目】某兴趣小组利用下图装置进行二氧化碳的制取和部分性质实验,请回答下列问题:
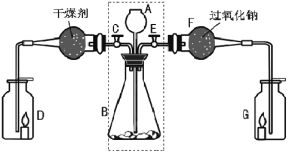
(1)关闭E打开C,从长颈漏斗A中加入液体与锥形瓶B中固体接触,即有二氧化碳气体产生。观察到D中的蜡烛慢慢熄灭,说明二氧化碳具有____________的性质。写出实验室制取二氧化碳的化学方程___________。
(2)关闭C打开E,则观察到G中的蜡烛燃烧得更旺,说明有氧气生成。
[查阅资料]二氧化碳能与过氧化钠(![]() )反应生成碳酸钠和氧气。
)反应生成碳酸钠和氧气。
[实验探究]要检验反应后F中的固体物质含有碳酸钠,可取少量反应后F中固体物质于试管中,滴入盐酸,观察到有气泡产生;用蘸有澄清石灰水的玻璃片放在试管口,观察到澄清石灰水变浑浊,写出该反应的化学方程式_________________。
[实验结论]二氧化碳与过氧化钠反应的化学方程式为____________________。
[拓展联系]某同学用一团棉花包裹过氧化钠并滴入几滴水,发现棉花团燃烧,说明过氧化钠也能和水反应生成氧气且反应一定___________(选填放热或吸热)。
【答案】(1)不燃烧不支持燃烧;![]() ;
;
(2)![]() ;
;![]() ;放热;
;放热;
【解析】
试题分析:(1)蜡烛熄灭说明二氧化碳不燃烧不支持燃烧;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,据此写出化学方程式;(2)碳酸盐和酸反应会生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊,该反应是氢氧化钙和二氧化碳反应生成碳酸钙和水;根据二氧化碳能与过氧化钠反应生成碳酸钠和氧气书写化学方程式;根据物质燃烧的条件可以得出反应是放热的;

练习册系列答案
相关题目