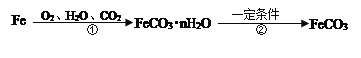题目内容
【题目】为探究分子的运动及影响分子运动速率的因素,某同学设计了以下三种实验方案,请回答有关问题
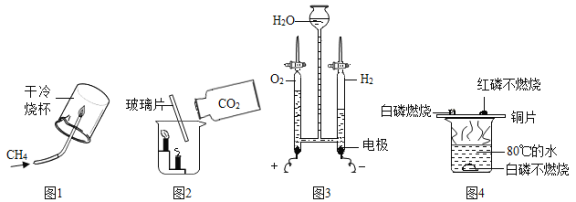
(实验方案一)如图1。
①观察到的实验现象是_____;
②该方案的不足之处是_____。(说出一点即可)
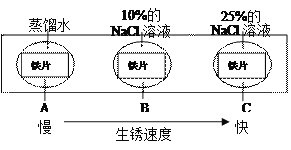
(实验方案二)如图2、图3。
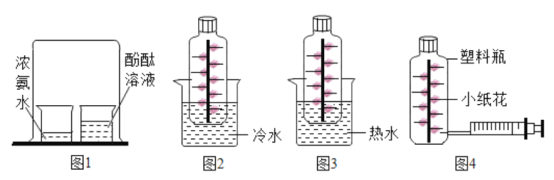
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
①观察到的现象是_____;
②图2、图3采用对照实验的方法,变量只有一个,被控制的量有多个,请说出4个被控制的量_____。
③若图4中的小纸花上喷有_____,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
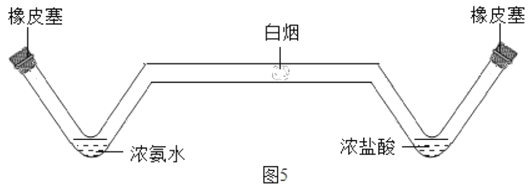
(实验方案三)如图5
用长柄V形玻璃管进行实验,向左、右两端的V形玻璃管口分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。
①过一会儿后,从图5中观察到有白烟产生且位置偏右,说明_____。
②图5中生成白烟的反应为化合反应,其化学方程式为_____。
(实验结论)上述实验证明:分子是不断运动的,且分子的运动速率与_____有关。(说出一点即可)
【答案】酚酞溶液变红色 ;没有设计对比实验 。小纸花由下而上依次变红色,并且图3比图2变色快 ;塑料瓶的材质、大小、形状完全相同;小纸花大小和形状相同;小纸花上都均匀喷有酚酞溶液;用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水 。石蕊溶液 ,氯化氢和氨气发生了化学反应,氨分子运动的比氯化氢分子运动的快 。NH3+HCl=NH4Cl 。相对分子质量
【解析】
微观粒子是不断运动的,温度越高运动的越快;显碱性溶液能使酚酞试液变红色,显酸性溶液能使石蕊试液变红色;氨气和氯化氢反应生成氯化铵。
【实验方案一】
①观察到的实验现象是酚酞试液变红色;②该方案的不足之处是没有设计对比实验,不能排除空气中的物质使酚酞溶液变色。
【实验方案二】
①观察到的现象是小纸花由下而上依次变红色,并且图3比图2变色快;②4个被控制的量是塑料瓶的材质、大小、形状完全相同;小纸花大小和形状相同;小纸花上都均匀喷有酚酞溶液;用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水;③若图4中的小纸花上喷有石蕊溶液,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
【实验方案三】
①过一会儿后,从图5中观察到有白烟产生且位置偏右,说明氯化氢和氨气发生了化学反应,氨分子运动的比氯化氢分子运动的快;②图5中生成白烟,是因为氨气和氯化氢反应生成了氯化铵,反应的化学方程式为:NH3+HCl=NH4Cl。
上述实验证明:分子是不断运动的,且分子的运动速率与相对分子质量有关,即相对分子质量越小,运动的速率越快。

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案【题目】下表是NaCl和Na2CO3在不同温度下的溶解度,下列说法中不正确的是( )
温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解度/g | NaCl | 35.0 | 35.5 | 36.0 | 36.5 | 37.0 |
Na2CO3 | 6.0 | 10.0 | 18.0 | 36.5 | 50.0 | |
A. 两种物质溶解度相等的温度在30℃
B. 生活在盐碱湖附近的人们习惯“夏天晒盐、冬天捞碱”
C. 40℃时,5gNaCl中加10g水可得溶质质量分数为26.3%的溶液
D. 40℃时,9g Na2CO3中加20g水,充分溶解后再降温到10℃,析出固体的质量为7g
【题目】通过化学变化可以制备物质。
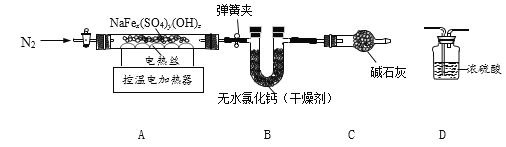
(1)某兴趣小组欲用200 g 4%的氢氧化钠溶液吸收二氧化碳制备碳酸钠,反应的化学方程式是___;若要将提供的氢氧化钠全部转化为碳酸钠,请列出计算需二氧化碳质量(x)的比例式_____;
(2)在实验中,该小组同学发现,要定量控制通入氢氧化钠溶液中二氧化碳气体的质量,难以操作。请分析若通入二氧化碳气体的量不足时会导致产物中混有的杂质是_____;
(3)查阅资料:
Na2CO3+CO2+H2O===2NaHCO3;NaHCO3+NaOH===Na2CO3+H2O;
该小组同学将制备方案改进如下:
步骤 | 实验操作 | 实验目的 |
一 | 将200g 4%的NaOH溶液分为两等份 | / |
二 | ①_____ | 将其中一份溶液中的NaOH全部转化为NaHCO3 |
三 | 将步骤二所得溶液小心煮沸1~2分钟 | ②___ |
四 | ③___ | 将NaHCO3全部转化为Na2CO3 |
(4)假设每步转化都完全,该小组同学利用改进后的方案制取的碳酸钠质量m1=___g;经老师指导,该小组同学将步骤四反应后的溶液蒸干并充分灼烧得到碳酸钠粉末的质量为m2g,发现m1=m2,由此证明他们的方案改进成功。