��Ŀ����
����Ŀ���������ƣ�Na2O2����һ�ֹ���������ˮ��Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2H2O�T4NaOH+O2����������Ϊ19.6g�IJ�����Na2O2��ֻ����NaOH���ʣ����뵽87.6gˮ�У�ǡ����ȫ��Ӧ��������Һ������Ϊ104g��ˮ�Ļӷ����Բ��ƣ�������㣺
��1����������������Ϊg��
��2����Ӧ��������Һ�����ʵ�����g��
��3����������Һϡ�ͳ����ʵ���������Ϊ10%����Һ�����ˮ������g��
���𰸡�
��1��3.2
��2��20
��3��96
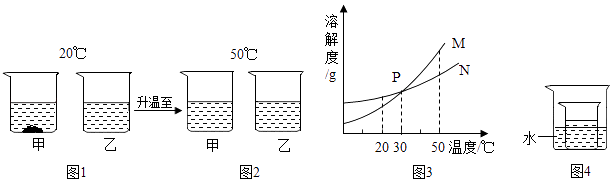
���������⣺��1����������������Ϊ19.6g+87.6g��104g=3.2g�����3.2����2����μӷ�Ӧ�Ĺ������Ƶ�����Ϊx�������������Ƶ�����Ϊy��
2Na2O2+2H2O�T | 4NaOH+ | O2�� |
156 | 160 | 32 |
x | y | 3.2g |
![]() ��
��
x=15.6g��y=16g��
��Һ�����ʵ�����Ϊ��19.6g��15.6g+16g=20g
�𰸣�20����3������Ҫ����ˮ������Ϊz��
20g�£�104g+z��=10%
z=96g
�𰸣�96��
�����㾫�������ո��ݻ�ѧ��Ӧ����ʽ�ļ����ǽ����ĸ�������Ҫ֪�������ʼ�������=ϵ������Է�������֮�ȣ�

����Ŀ��Ϊ�˲ⶨҺ�����б��飨C3H8������������ʱ��ȼ�ղ����һ�����ı������������һ����յ���������ȼ����÷�Ӧǰ������ʵ��������±���
���� | ���� | ���� | ˮ | ������̼ | X |
��Ӧǰ����/g | 4.4 | 12.8 | 0 | 0 | 0 |
��Ӧ������/g | 0 | 0 | 7.2 | 4.4 | a |
�����ж���ȷ���ǣ� ��
A.����a��ֵΪ4.6
B.X�����Ǹ÷�Ӧ�Ĵ���
C.X���ܺ�����Ԫ��
D.Xֻ��̼��Ԫ��