��Ŀ����
����Ŀ��Ϊ�ⶨ�����������ĺ�����С��ͬѧ����������·�����ѡ��ʵ���ݻ�Ϊ40mL���Թ�����Ӧ�������������İ������Թܣ�����Ƥ�������Թܣ�ͨ��������ʵ���ݻ�Ϊ60mL�һ����Ժܺõ���Ͳע���������ͼ��ʵ��װ�ã������ʵ���ܹ�����С���������������У��Ұ�����ռ����뵼���ڵ�����������Բ��ƣ���ش��������⣺ 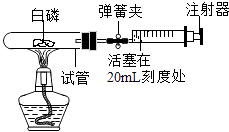
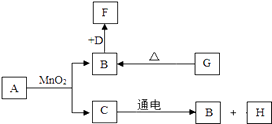
��1������ȼ�յĻ�ѧ����ʽΪ ��
��2��ʵ��ǰ�����ɼУ���ע��������ǰ�ش�20mL�̶ȴ�����15mL�̶ȴ���Ȼ���ɿ��֣����������ܷ���20mL�̶ȴ�����˵���� ��
��3�����ȼн����ɼУ��þƾ��Ƽ��Ȱ��ף�ȼ�ս������ȵ��Թ���ȴ�����ɿ����ɼУ��ɹ۲쵽ע��������ͣ����mL�̶ȴ���
��4������ʹ�õ��ɼУ��þƾ��Ƽ��Ȱ��ף���ַ�Ӧֱ��ȼ�ս������Թ���ȴ������ʵ������пɹ۲쵽������Ϊ���� ��
��5������С�����������ʵ�飬ʵ�ʿ�������������������Σ�գ����ʵ��ʧ�ܣ����磺 ��
���𰸡�
��1��4P+5O2 ![]() ?2P2O5
?2P2O5
��2��װ�õ������Ժ�
��3��12
��4������ȼ�գ��������̣������������ƶ��������ȶ���Լ8mL�Ŀ̶�����
��5�������������Թܱ��ѡ�ע��������������
���������⣺��1������ȼ�յĻ�ѧ����ʽΪ��4P+5O2 ![]() 2P2O5 �� ��2�����ɼУ���ע��������ǰ�ش�20mL�̶ȴ�����15mL�̶ȴ���Ȼ���ɿ��֣����������ܷ�����20mL�̶ȴ�����˵������װ�ö���©������3�����ȼн����ɼУ��þƾ��Ƽ��Ȱ��ף���ʱ����ȼ�����ĵ���ֻ���Թ��ڵ�����Ϊ40mL��
2P2O5 �� ��2�����ɼУ���ע��������ǰ�ش�20mL�̶ȴ�����15mL�̶ȴ���Ȼ���ɿ��֣����������ܷ�����20mL�̶ȴ�����˵������װ�ö���©������3�����ȼн����ɼУ��þƾ��Ƽ��Ȱ��ף���ʱ����ȼ�����ĵ���ֻ���Թ��ڵ�����Ϊ40mL�� ![]() =8mL�����Ի���Ӧͣ��20mL��8mL=12mL�Ŀ̶ȴ�����4������ʹ�õ��ɼУ��þƾ��Ƽ��Ȱ��ף�����ʵ�����ĵ������Թ�40mL��ע������20mL������Ϊ��40mL+20mL����
=8mL�����Ի���Ӧͣ��20mL��8mL=12mL�Ŀ̶ȴ�����4������ʹ�õ��ɼУ��þƾ��Ƽ��Ȱ��ף�����ʵ�����ĵ������Թ�40mL��ע������20mL������Ϊ��40mL+20mL���� ![]() =12mL�����Ի���Ӧͣ��20mL��12mL=8mL�Ŀ̶ȴ�����5����Ϊ�������ܱ�������ȼ�ղ�������ʹ�������ͣ����ܻ�ʹ�����������Թܱ��ѡ���ʹ�õ��ɼп��ܻ�ʹע�������������ȣ����ʵ��ʧ�ܣ�
=12mL�����Ի���Ӧͣ��20mL��12mL=8mL�Ŀ̶ȴ�����5����Ϊ�������ܱ�������ȼ�ղ�������ʹ�������ͣ����ܻ�ʹ�����������Թܱ��ѡ���ʹ�õ��ɼп��ܻ�ʹע�������������ȣ����ʵ��ʧ�ܣ�
���Դ��ǣ���1��4P+5O2 ![]() 2P2O5����2��װ�õ������Ժã���3��12����4������ȼ�գ��������̣������������ƶ��������ȶ���Լ8mL�Ŀ̶����ϣ���5�������������Թܱ��ѡ�ע�������������ȣ�
2P2O5����2��װ�õ������Ժã���3��12����4������ȼ�գ��������̣������������ƶ��������ȶ���Լ8mL�Ŀ̶����ϣ���5�������������Թܱ��ѡ�ע�������������ȣ�
�����㾫�������ڱ��⿼�����д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ����Ҫ�˽�ע�⣺a����ƽ b������ c�����Ų��ܵó���ȷ�𰸣�