题目内容
把一定量的二氧化碳气体通入95.6g的氢氧化钠溶液中,完全反应后,溶液的质量是100g,(1)参加反应的二氧化碳是
分析:(1)反应的生成物中无气体或沉淀生成,根据质量守恒定律,反应后所得溶液的质量=氢氧化钠溶液质量+二氧化碳质量.
(2)反应后所得溶液为碳酸钠溶液,应根据参加反应的二氧化碳的质量计算反应生成的碳酸钠的质量,进一步求得碳酸钠溶液的溶质质量分数
(2)反应后所得溶液为碳酸钠溶液,应根据参加反应的二氧化碳的质量计算反应生成的碳酸钠的质量,进一步求得碳酸钠溶液的溶质质量分数
解答:解:
(1)参加反应的二氧化碳的质量为:100g-95.6g=4.4g故答案为:4.4
(2)设生成碳酸钠的质量为x
2NaOH+CO2=Na2CO3+H2O(1分)
44 106
4.4g x
44:106=4.4g:x
解之得:x=10.6g
反应后所得溶液的质量分数=
×100%=10.6%
答:反应后所得溶液的质量分数为10.6%;故答案为:10.6%
(1)参加反应的二氧化碳的质量为:100g-95.6g=4.4g故答案为:4.4
(2)设生成碳酸钠的质量为x
2NaOH+CO2=Na2CO3+H2O(1分)
44 106
4.4g x
44:106=4.4g:x
解之得:x=10.6g
反应后所得溶液的质量分数=
| 10.6g |
| 100g |
答:反应后所得溶液的质量分数为10.6%;故答案为:10.6%
点评:95.6g为氢氧化钠溶液的质量,不是纯净物氢氧化钠的质量,所以不能使用该质量利用化学方程式进行计算.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
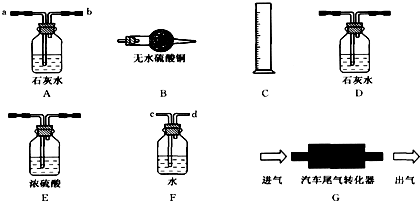
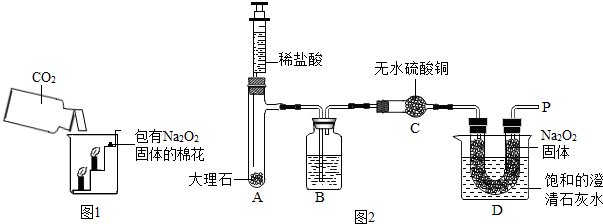
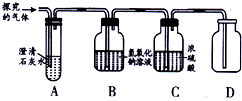 碳及许多含碳化合物不充分燃烧都要产生一氧化碳,一氧化碳是一种污染空气的有毒气体,它使人中毒的原因是
碳及许多含碳化合物不充分燃烧都要产生一氧化碳,一氧化碳是一种污染空气的有毒气体,它使人中毒的原因是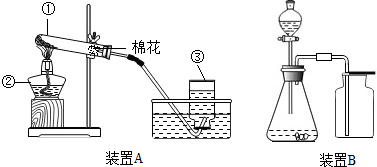 实验室常用于制取氧气的方法有:
实验室常用于制取氧气的方法有: 12CO2+4CO+18H2O(其中X代表汽油的化学式),请你写出X的化学式________.
12CO2+4CO+18H2O(其中X代表汽油的化学式),请你写出X的化学式________.