题目内容
(2005?玄武区一模)随着汽车工业的飞速发展,汽车尾气作为一种重要的空气污染源,越来越受到世界各国的普遍关注.
(1)汽车通常用汽油做燃料,若汽油燃烧时供氧不足,就会产生有毒气体一氧化碳,反应的化学方程式为:
2X+23O2
12CO2+4CO+18H2O(其中X代表汽油的化学式),请你写出X的化学式
(2)汽车尾气中主要的有害气体是CO和NO,为了减少空气污染,通常在汽车的排气管上安装一个“催化转化器”(用铂、钯合金做催化剂),使它们转化为参与大气生态循环的二氧化碳和氮气.请写出转化器中发生反应的化学反应方程式
(3)除了用上述“催化转化器”方法减少汽车尾气污染外,请你为环保部门提供一些关于防止汽车尾气污染的建议(至少两条)
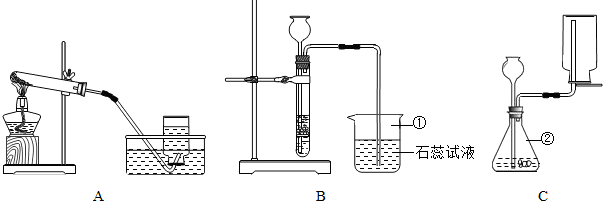
(4)杨华同学为了证明汽车尾气中含有CO2、CO、H2O,并测定出转化后所得氮气的体积(假设每步反应都完全,进入转化器的气体要求干燥,假设汽车尾气中只含CO2、CO、H2O、NO),在环保科研人员的帮助下,取来一定量的汽车尾气进行实验.(白色的无水硫酸铜与水反应生成蓝色的硫酸铜晶体)
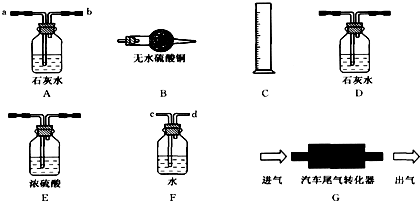
①现有如图所示装置,请你为该同学把实验装置按气流方向从左至右连接好(仪器不重复使用,用装置序号填空):汽车尾气接
②A装置应从
③写出A中发生反应的化学方程式
(5)如果该同学取来的汽车尾气质量为100g,按上题实验要求来做,已知经过“催化转化器”转化后的气体通过盛石灰水装置,该装置反应前的质量为303.50g,反应后的质量为303.94g.请你计算所取的汽车尾气中CO的质量分数.(相对原子质量:H-1 C-12 O-16 Ca-40)
(1)汽车通常用汽油做燃料,若汽油燃烧时供氧不足,就会产生有毒气体一氧化碳,反应的化学方程式为:
2X+23O2
| ||
C8H18
C8H18
.(2)汽车尾气中主要的有害气体是CO和NO,为了减少空气污染,通常在汽车的排气管上安装一个“催化转化器”(用铂、钯合金做催化剂),使它们转化为参与大气生态循环的二氧化碳和氮气.请写出转化器中发生反应的化学反应方程式
2CO+2NO
2CO2+N2
| ||
2CO+2NO
2CO2+N2
.
| ||
(3)除了用上述“催化转化器”方法减少汽车尾气污染外,请你为环保部门提供一些关于防止汽车尾气污染的建议(至少两条)
改进发动机燃烧方式
改进发动机燃烧方式
;使用其它清洁能源
使用其它清洁能源
.(4)杨华同学为了证明汽车尾气中含有CO2、CO、H2O,并测定出转化后所得氮气的体积(假设每步反应都完全,进入转化器的气体要求干燥,假设汽车尾气中只含CO2、CO、H2O、NO),在环保科研人员的帮助下,取来一定量的汽车尾气进行实验.(白色的无水硫酸铜与水反应生成蓝色的硫酸铜晶体)
①现有如图所示装置,请你为该同学把实验装置按气流方向从左至右连接好(仪器不重复使用,用装置序号填空):汽车尾气接
B
B
接A
A
接E
E
接G
G
接D
D
接F
F
接C
C
.
②A装置应从
a
a
(填小写字母)端进气,F装置应从d
d
(填小写字母)端进气.③写出A中发生反应的化学方程式
CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Ca(OH)2═CaCO3↓+H2O
.(5)如果该同学取来的汽车尾气质量为100g,按上题实验要求来做,已知经过“催化转化器”转化后的气体通过盛石灰水装置,该装置反应前的质量为303.50g,反应后的质量为303.94g.请你计算所取的汽车尾气中CO的质量分数.(相对原子质量:H-1 C-12 O-16 Ca-40)
分析:(1)根据化学反应前后原子的种类和数目进行解答;
(2)根据CO和NO在铂、钯合金做催化剂的情况下生成二氧化碳和氮气进行解答;
(3)根据汽车尾气的排放易造成空气污染,除了使用催化转化器处理尾气的角度还可以从改变燃料方面进行解答;
(4)根据验证和除杂的顺序进行解答;
(5)根据装置质量增加的为二氧化碳的质量进行解答.
(2)根据CO和NO在铂、钯合金做催化剂的情况下生成二氧化碳和氮气进行解答;
(3)根据汽车尾气的排放易造成空气污染,除了使用催化转化器处理尾气的角度还可以从改变燃料方面进行解答;
(4)根据验证和除杂的顺序进行解答;
(5)根据装置质量增加的为二氧化碳的质量进行解答.
解答:解:(1)根据化学反应前后原子的种类和数目,由2X+23O2
12CO2+4CO+18H2O可知,X的化学式为C8H18;故填:C8H18;
(2)CO和NO在铂、钯合金做催化剂的情况下生成二氧化碳和氮气,发生反应的化学反应方程式2CO+2NO
2CO2+N2;故填:2CO+2NO
2CO2+N2;
(3)为防止汽车的尾气污染空气,除了使用催化转化器处理尾气的角度还可以从改变燃料方面等措施,所以本题答案为:改进发动机燃烧方式、使用无铅汽油、使用其它清洁能源等;故填:改进发动机燃烧方式;使用其它清洁能源;
(4)①验证水和二氧化碳,要先验证水再验证二氧化碳,所以气体先通过B装置验证水,再通过A装置验证二氧化碳,进入转化器的气体要求干燥,所以气体再通过E装置进行干燥,然后通过G装置,吸收生成二氧化碳通过D装置,测定氮气的体积根据氮气难溶于水,所以通过F装置,将装置的水排进量筒中,进入量筒内水的体积等于氮气的体积,所以气体先后通过F和C,所以连接顺序为汽车尾气→B→A→E→G→D→F→C;故填:B;A;E;G;D;F;C;
②A装置验证二氧化碳,所以从a端进气;装置F是将水排出收集氮气,所以从d端进气;故填:a;d;
③二氧化碳与氢氧化钙在常温下反应生成碳酸钙和水,反应的化学方程式为为:CO2+Ca(OH)2═CaCO3↓+H2O;故填:CO2+Ca(OH)2═CaCO3↓+H2O;
(5)设一氧化碳的质量为x.
二氧化碳的质量为303.94g-303.50g=0.44g
2CO+2NO
2CO2+N2
56 88
x 0.44g
=
x=0.28g
汽车尾气中CO的质量分数=
×100%=0.28%
答:汽车尾气中CO的质量分数为0.28%.
| ||
(2)CO和NO在铂、钯合金做催化剂的情况下生成二氧化碳和氮气,发生反应的化学反应方程式2CO+2NO
| ||
| ||
(3)为防止汽车的尾气污染空气,除了使用催化转化器处理尾气的角度还可以从改变燃料方面等措施,所以本题答案为:改进发动机燃烧方式、使用无铅汽油、使用其它清洁能源等;故填:改进发动机燃烧方式;使用其它清洁能源;
(4)①验证水和二氧化碳,要先验证水再验证二氧化碳,所以气体先通过B装置验证水,再通过A装置验证二氧化碳,进入转化器的气体要求干燥,所以气体再通过E装置进行干燥,然后通过G装置,吸收生成二氧化碳通过D装置,测定氮气的体积根据氮气难溶于水,所以通过F装置,将装置的水排进量筒中,进入量筒内水的体积等于氮气的体积,所以气体先后通过F和C,所以连接顺序为汽车尾气→B→A→E→G→D→F→C;故填:B;A;E;G;D;F;C;
②A装置验证二氧化碳,所以从a端进气;装置F是将水排出收集氮气,所以从d端进气;故填:a;d;
③二氧化碳与氢氧化钙在常温下反应生成碳酸钙和水,反应的化学方程式为为:CO2+Ca(OH)2═CaCO3↓+H2O;故填:CO2+Ca(OH)2═CaCO3↓+H2O;
(5)设一氧化碳的质量为x.
二氧化碳的质量为303.94g-303.50g=0.44g
2CO+2NO
| ||
56 88
x 0.44g
| 56 |
| x |
| 88 |
| 0.44g |
x=0.28g
汽车尾气中CO的质量分数=
| 0.28g |
| 100g |
答:汽车尾气中CO的质量分数为0.28%.
点评:本题主要考查化学方程式的书写方法和相关方面的计算,书写化学方程式时要遵循质量守恒定律.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目