题目内容
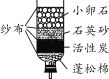
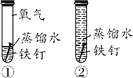
【题目】如图所示,向盛有铁钉的试管中注入稀盐酸,实验结束后铁钉连同废液一起倒入指定的带有纱网的烧杯中,实验中发现纱网上的铁钉很容易生锈,生锈应该是铁钉与________共同作用的结果。

(提出问题)为什么纱网上的铁钉更容易生锈呢?
(小明猜想)纱网上的铁钉表面可能有盐酸,是不是酸能促进铁钉生锈呢?
(实验验证)
(1)从纱网上取5枚干燥的铁钉放入试管中,加水没过铁钉,轻轻的摇动试管后,把液体转移入小烧杯,测定该液体的pH,测定方法是_______,结果pH=5。
(2)请你设计一个对比实验,直观地证明酸能促进铁钉生锈:___________。
(拓展延伸)生锈的铁钉要想重复使用需要除掉铁锈。小明把生锈铁钉泡在废弃的稀盐酸中,很快发现铁锈消失,溶液变成________色,反应的化学方程式是___________。小明继续观察,发现溶液中又产生了许多气泡,他猜想是产生了氢气,于是收集了一试管的该气体,他又做了实验:____。证明该气体就是氢气。
(反思交流)为保证铁钉重复利用,倒在纱网上的铁钉应该________。
【答案】氧气和水 用玻璃棒蘸取待测液,滴在pH试纸上,和标准比色卡比较 在带纱网的烧杯内盛水,纱网上放铁钉,与实验中的纱网上的铁钉比较 黄 ![]() 点燃气体产生淡蓝色火焰 用水冲洗后晾干保存
点燃气体产生淡蓝色火焰 用水冲洗后晾干保存
【解析】
铁生锈的实质是铁与氧气和水共同作用的结果。
【实验验证】(1)用pH试纸测定溶液pH的正确方法是:用玻璃棒蘸取待测液,滴在pH试纸上,和标准比色卡比较,读出数值。(2)纱网上的铁钉是接触酸的,所以要想通过对比实验证明酸能促进铁钉生锈,还需要在其它条件相同的情况下做一个不接触酸的实验,即在带纱网的烧杯内盛水,纱网上放铁钉。【拓展延伸】铁锈的成分为氧化铁,氧化铁与盐酸反应生成氯化铁和水,氯化铁溶液呈黄色,所以生锈铁钉泡在稀盐酸中会看到铁锈消失,溶液变成黄色,反应的化学方程式为Fe2O3+6HCl=== 2FeCl3+3H2O;当溶液中产生气泡时,说明盐酸过量,铁锈反应完后铁又与盐酸反应,证明生成气体为氢气的方法是利用氢气的可燃性。【反思交流】为保证铁钉重复利用,要防止生锈,所以铁钉在使用后洗净晾干后保存。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案