题目内容
现有HCl与CaCl2的混合溶液,为了测定混合溶液中HCl和CaCl2的质量分数,设计了如下实验方案: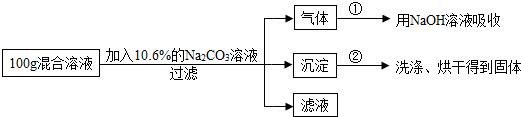
【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,生成 的质量为4.4g.
(2)m= .
(3)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?.(不考虑过滤中的损失,计算结果保留到小数点后一位.)

【实验数据】上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,共记录了两组实验数据:第①组,气体吸收完全后,NaOH溶液质量增加4.4g;第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.
根据实验设计及有关数据进行分析与计算:
(1)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应后,生成
(2)m=
(3)上述实验中100g混合溶液与mg溶质的质量分数为10.6%的Na2CO3溶液恰好完全反应,经过滤后所得“滤液”中溶质的质量分数为多少?.(不考虑过滤中的损失,计算结果保留到小数点后一位.)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)由题意可以知道生成二氧化碳的质量为4.4g;
(2)利用二氧化碳的质量,可以据此结合碳酸钠和盐酸反应的化学方程式求算出碳酸钠的质量,然后求出其溶液质量即可.根据图中数据可以知道生成沉淀的质量为10g,可以据此结合碳酸钠和氯化钙反应的化学方程式求算出碳酸钠的质量,然后求出其溶液质量即可.
(3)根据发生的化学反应可以知道反应后得到的滤液为氯化钠溶液,所以可以根据上述反应求算出氯化钠的质量,然后根据溶质的质量分数的计算公式求解即可.
(2)利用二氧化碳的质量,可以据此结合碳酸钠和盐酸反应的化学方程式求算出碳酸钠的质量,然后求出其溶液质量即可.根据图中数据可以知道生成沉淀的质量为10g,可以据此结合碳酸钠和氯化钙反应的化学方程式求算出碳酸钠的质量,然后求出其溶液质量即可.
(3)根据发生的化学反应可以知道反应后得到的滤液为氯化钠溶液,所以可以根据上述反应求算出氯化钠的质量,然后根据溶质的质量分数的计算公式求解即可.
解答:解:
(1)氢氧化钠溶液增加的质量即为碳酸钠和盐酸反应生成二氧化碳的质量,即为4.4g,
设与盐酸反应消耗碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
=
x=10.6g
=
y=11.7g
设与氯化钙反应消耗碳酸钠的质量为z,生成氯化钠的质量为w,根据图中数据可以知道生成沉淀碳酸钙的质量为10g
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100 117
z 10g w
=
z=10.6g
=
w=11.7g
(2)盐酸消耗碳酸钠溶液的质量为:
=100g,氯化钙消耗碳酸钠溶液的质量为:
=100g,gu m的值为100g+100g=200g;
(3)根据发生的化学反应可以知道反应后得到的滤液为氯化钠溶液,
滤液中溶质氯化钠的质量为:11.7g+11.7g=23.4g,
所以反应后溶液的质量为:100g+100g+100g-4.4g-10g=285.6g
故反应后滤液中溶质的质量分数为:
×100%=8.2%;
答案:
(1)二氧化碳
(2)200g
(3)反应后滤液中溶质的质量分数为8.2%.
(1)氢氧化钠溶液增加的质量即为碳酸钠和盐酸反应生成二氧化碳的质量,即为4.4g,
设与盐酸反应消耗碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
| 106 |
| 44 |
| x |
| 4.4g |
x=10.6g
| 117 |
| 44 |
| y |
| 4.4g |
y=11.7g
设与氯化钙反应消耗碳酸钠的质量为z,生成氯化钠的质量为w,根据图中数据可以知道生成沉淀碳酸钙的质量为10g
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100 117
z 10g w
| 106 |
| 100 |
| z |
| 10g |
z=10.6g
| 100 |
| 117 |
| 10g |
| w |
w=11.7g
(2)盐酸消耗碳酸钠溶液的质量为:
| 10g |
| 10.6% |
| 10g |
| 10.6% |
(3)根据发生的化学反应可以知道反应后得到的滤液为氯化钠溶液,
滤液中溶质氯化钠的质量为:11.7g+11.7g=23.4g,
所以反应后溶液的质量为:100g+100g+100g-4.4g-10g=285.6g
故反应后滤液中溶质的质量分数为:
| 23.4g |
| 285.6g |
答案:
(1)二氧化碳
(2)200g
(3)反应后滤液中溶质的质量分数为8.2%.
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地解答即可.

练习册系列答案
相关题目
 “益达”口香糖中的木糖醇(化学式为C5H12O5)是一种新型甜昧剂.下列关于木糖醇的说法错误的是( )
“益达”口香糖中的木糖醇(化学式为C5H12O5)是一种新型甜昧剂.下列关于木糖醇的说法错误的是( )| A、木糖醇中C、H、O三种元素的原子个数比为5:12:5 |
| B、一个木糖醇分子中含有22个原子 |
| C、木糖醇属于有机化合物 |
| D、木糖醇是由多个原子构成的纯净物 |
下列变化中,前者是化学变化,后者是物理变化的是( )
| A、锅炉爆炸 海水晒盐 |
| B、牛奶变酸 米酿成醋 |
| C、矿石粉碎 食物腐烂 |
| D、蜡烛燃烧 酒精挥发 |
下列物质燃烧时发出淡蓝色火焰的是( )
| A、硫在空气中燃烧 |
| B、碳在氧气中燃烧 |
| C、硫在氧气中燃烧 |
| D、铁在氧气中燃烧 |