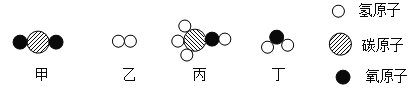
��Ŀ����
����Ŀ����ҵ���Ʊ�SO3�ķ�ӦΪ��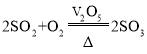 .һ�������£���һ�ܱ�������Ͷ��SO2��O2��SO3��V2O5�������ʣ��ڲ�ͬʱ���ø����ʵ��������±���ʾ��
.һ�������£���һ�ܱ�������Ͷ��SO2��O2��SO3��V2O5�������ʣ��ڲ�ͬʱ���ø����ʵ��������±���ʾ��
���� | �� | �� | �� | �� |
t1������/g | 100 | 5 | 80 | 5 |
t2������/g | 60 | 55 | a | b |
t3������/g | 40 | c | d | 5 |
��1����ҵ���Ʊ�SO3�����У��μӷ�Ӧ��SO2��O2���Ӹ�����Ϊ________���÷�Ӧ����________�����������������ֽ�������Ӧ��
��2��������c_________,���ʱ���_______������SO2������O2������SO3������V2O5������
���𰸡�2:1 ���Ϸ�Ӧ 80 O2
��������
��1����ҵ���Ʊ�SO3�����У����ݷ�Ӧ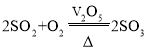 ��֪�μӷ�Ӧ��SO2��O2���Ӹ�����Ϊ2:1���÷�Ӧ���ϡ����һ�������������ڻ��Ϸ�Ӧ��
��֪�μӷ�Ӧ��SO2��O2���Ӹ�����Ϊ2:1���÷�Ӧ���ϡ����һ�������������ڻ��Ϸ�Ӧ��
��2������Ӧǰ���������䣬���������������ҷ�Ӧ�����������������������������Ӧ��������С���Ƿ�Ӧ��ҡ����������ǣ�55g-5g������100g-60g��=5��4�����ݷ�Ӧ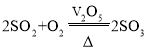 ��֪����������Ͷ���������������5��4������Ƕ������������������Ӧ��100g��40g��ʱ�������ҵ�����Ϊx������5:4=x��60��x=75g����c=75g+5g=80g��
��֪����������Ͷ���������������5��4������Ƕ������������������Ӧ��100g��40g��ʱ�������ҵ�����Ϊx������5:4=x��60��x=75g����c=75g+5g=80g��
��������cΪ80�����ʱ���O2��