题目内容
22、某学校化学实验室要用98%的浓硫酸(密度为1.84g/cm3)配制1L30%的硫酸溶液(密度为1.22g/cm3).配制1L30%的硫酸溶液.
①计算
需要98%的浓硫酸的体积为
②量取
③稀释
稀释浓硫酸时的正确操作是
①计算
需要98%的浓硫酸的体积为
203
mL,需加水的体积为846
mL(水的密度近似看作1g/cm3,计算结果取整数).②量取
③稀释
稀释浓硫酸时的正确操作是
一定要把浓硫酸沿器壁慢慢注入水里,并不断搅拌
.分析:①根据加水稀释前后溶液中溶质质量不变,由稀释后所得稀硫酸计算需要浓硫酸的体积和所加水的体积;
③根据浓硫酸溶解时会放出大量的热,为防止放出的热量造成液体溅出,稀释时应严格遵循规定进行溶解.
③根据浓硫酸溶解时会放出大量的热,为防止放出的热量造成液体溅出,稀释时应严格遵循规定进行溶解.
解答:解:①设需要浓硫酸的质量为x
x×98%=1L×1000×1.22g/cm3×30%
x=373.5g
则需要98%的浓硫酸的体积=373.5g÷1.84g/cm3=203mL
需加水的体积=1L×1000×1.22g/cm3-373.5g=846g合846mL
③为防止浓硫酸溶解时放出大量的热不能及时扩散而引起液体飞溅,在稀释浓硫酸时一定要把浓硫酸沿器壁慢慢注入水里,并不断搅拌;
故答案为:
(1)203;846;
(2)一定要把浓硫酸沿器壁慢慢注入水里,并不断搅拌.
x×98%=1L×1000×1.22g/cm3×30%
x=373.5g
则需要98%的浓硫酸的体积=373.5g÷1.84g/cm3=203mL
需加水的体积=1L×1000×1.22g/cm3-373.5g=846g合846mL
③为防止浓硫酸溶解时放出大量的热不能及时扩散而引起液体飞溅,在稀释浓硫酸时一定要把浓硫酸沿器壁慢慢注入水里,并不断搅拌;
故答案为:
(1)203;846;
(2)一定要把浓硫酸沿器壁慢慢注入水里,并不断搅拌.
点评:在稀释浓硫酸时一定要把浓硫酸沿器壁慢慢注入水里,切不可把水倒入浓硫酸中.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
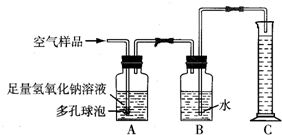 A.某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含SO2的废气和含H2SO4的酸性废水.当地的其他工厂和居民均用煤炭作燃料.只要下雨就下酸雨,对该镇环境造成极大破坏.
A.某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含SO2的废气和含H2SO4的酸性废水.当地的其他工厂和居民均用煤炭作燃料.只要下雨就下酸雨,对该镇环境造成极大破坏.