题目内容
 (2013?南昌)某厂排放的废水中含有碳酸钠,易造成环境污染.化学兴趣小组为该厂设计废水处理和利用的方案,进行了如下实验:取过滤后的水样200g,逐滴加入稀盐酸至恰好不再产生气体为止,反应过程中生成气体与所加稀盐酸的质量关系如图所示.请回答下列问题(不考虑水样中杂质的影响):
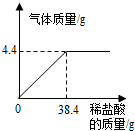
(2013?南昌)某厂排放的废水中含有碳酸钠,易造成环境污染.化学兴趣小组为该厂设计废水处理和利用的方案,进行了如下实验:取过滤后的水样200g,逐滴加入稀盐酸至恰好不再产生气体为止,反应过程中生成气体与所加稀盐酸的质量关系如图所示.请回答下列问题(不考虑水样中杂质的影响):(1)反应生成CO2气体的质量是
4.4
4.4
g;(2)反应后生成氯化钠的质量是多少?(写出计算过程)
(3)农业上常用10%-20%的氯化钠溶液来选种.请通过列式计算判断:上述实验反应后所得溶液能否直接用于农业上选种?.
分析:(1)根据图象可判断最终生成二氧化碳的质量;
(2)根据二氧化碳的质量可以求出生成的氯化钠的质量;
(3)据溶质的质量分数=
×100%计算氯化钠溶液的溶质质量分数,氯化钠溶液的质量=反应前各组分的和-生成气体的质量,然后与农业上常用10%-20%的氯化钠溶液的质量分数进行比较作出判断.
(2)根据二氧化碳的质量可以求出生成的氯化钠的质量;
(3)据溶质的质量分数=
| 溶质的质量 |
| 溶液的质量 |
解答:解:(1)由图象可知反应后生成的二氧化碳的质量是4.4g;
(2)设生成的氯化钠的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
117 44
x 4.4g
=
,x=11.7g
(3)由图象可以看出,二者恰好反应时消耗的稀盐酸的质量是38.4g,所以反应后溶液的质量是:200g+38.4g-4.4g=234g,溶质的质量分数是
×100%=5%<10%,所以不能直接用于农业上选种;
故答案为:(1)4.4;(2)反应后生成氯化钠11.7g;(3)实验反应后所得溶液不能直接用于农业上选种.
(2)设生成的氯化钠的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
117 44
x 4.4g
| 117 |
| x |
| 44 |
| 4.4g |
(3)由图象可以看出,二者恰好反应时消耗的稀盐酸的质量是38.4g,所以反应后溶液的质量是:200g+38.4g-4.4g=234g,溶质的质量分数是
| 11.7g |
| 234g |
故答案为:(1)4.4;(2)反应后生成氯化钠11.7g;(3)实验反应后所得溶液不能直接用于农业上选种.
点评:本题考查了依据图象分析获取信息,并进行解题的能力,图象的转折点通常是恰好完全反应的点,是解题的关键所在.

练习册系列答案
相关题目
 ”与“
”与“ 分别表示不同元素的原子.图中X处的粒子示意图是( )
分别表示不同元素的原子.图中X处的粒子示意图是( )
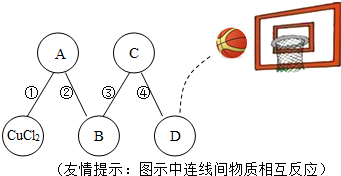 (2013?南昌)+物质王国举行一场趣味篮球赛.某对由铁、二氧化碳、稀硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成有效进攻.传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图.(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是
(2013?南昌)+物质王国举行一场趣味篮球赛.某对由铁、二氧化碳、稀硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成有效进攻.传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图.(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是