题目内容
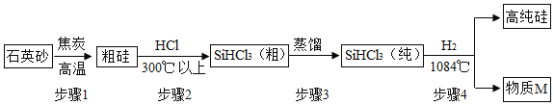
【题目】芯片的核心材料是高纯硅,下图是利用石英砂(主要成分SiO2)制取高纯硅的流程图,请回 答下列问题:
(1)SiO2与金刚石结构相似,则构成SiO2的粒子是__(填“分子”、“原子”或“离子”)。
(2)步骤 1 发生的反应为:SiO2+ 2C![]() Si + 2X↑,上述反应中 X 是______(填化学式),其中SiO2发生了______(填“氧化”或“还原”)反应。
Si + 2X↑,上述反应中 X 是______(填化学式),其中SiO2发生了______(填“氧化”或“还原”)反应。
(3)步骤 3 中“蒸馏”属于__(填“物理”或“化学”)变化。
(4)步骤 4 中物质 M 在该生产过程中可循环使用,写出步骤 4 反应的化学方程式:______。
【答案】原子 CO 还原 物理 SiHCl3+H2![]() Si+3HCl
Si+3HCl
【解析】
(1)金刚石是由原子构成的单质,二氧化硅与金刚石的结构相似,则二氧化硅也是由原子构成的,故填原子。
(2)由化学方程式可知,反应前出现了1个硅原子、2个氧原子和2个碳原子,反应后出现了1个硅原子,根据质量守恒定律的原因可知,尚缺的2个碳原子与2个氧原子存在于2X中,则1个X中含有1个碳原子和1个氧原子,即X的化学式为CO,故填CO;
由化学方程式可知,反应中二氧化硅失去氧,被还原为硅单质,即二氧化硅发生了还原反应,故填还原。
(3)蒸馏是将水与其中的可溶性杂质分离的过程,并没有生成新物质,属于物理变化,故填物理。
(4)由流程图可知,步骤4中的反应物中含有硅、氢、氯三种元素,生成的高纯硅中只含有硅元素,所以M中一定含有氢元素和氯元素,即M为氯化氢,则步骤4中的反应是三氯硅烷与氢气在高温的条件下反应生成高纯硅和氯化氢,故反应的化学方程式写为:SiHCl3+H2![]() Si+3HCl。
Si+3HCl。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
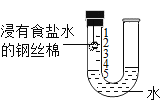
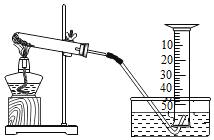
小学生10分钟应用题系列答案【题目】某兴趣小组对KClO3分解反应的催化剂进行探究,在相同的加热条件下,用如图装置完成表中实验,并记录相关数据填表中:
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mL O2所需时间/s |
实验1 | 5 | ﹣ | ﹣ | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
关于以上实验探宄,如下说法中不正确的是( )
A.设置实验1的目的是做对比实验
B.若维持加热条件不变,用实验1再收集50mL O2所需时间明显少于171s,原因是生成的KCl加快了反应
C.要比较KClO3分解反应中不同催化剂的催化效果,还可以测量相同时间内收集O2的体积
D.表中所列3种催化剂的催化效果最佳的是KCl