题目内容
每到冬天,市场上便有一种“热宝”出售,它是一个装有化学药品的小袋。使用时,撕去它的保护膜贴在身体上,不久便会产生热量。已知小袋中装有铁粉、碳粉和少量氯化钠。
(1)“热宝”使用前,取小袋内物质,加入稀硫酸中,发生反应的化学方程式为:
_________________________________________________________________________;
(2)“热宝”发热,其实是利用了铁粉与空气中的___________________反应放出的热量。“热宝”工作一段时间后失效,此时取小袋内物质,加入一定量的稀硫酸写出反应的化学方程式_________________________________________________,充分反应后过滤,则滤液中一定有的溶质是____________________(填写化学式)。
(1)“热宝”使用前,取小袋内物质,加入稀硫酸中,发生反应的化学方程式为:
_________________________________________________________________________;
(2)“热宝”发热,其实是利用了铁粉与空气中的___________________反应放出的热量。“热宝”工作一段时间后失效,此时取小袋内物质,加入一定量的稀硫酸写出反应的化学方程式_________________________________________________,充分反应后过滤,则滤液中一定有的溶质是____________________(填写化学式)。
(1) Fe + H2SO4 = FeSO4 + H2↑
(2) 水、氧气 3H2SO4 + Fe2O3 = Fe2(SO4)3 + 3H2O NaCl,Fe2(SO4)3
(2) 水、氧气 3H2SO4 + Fe2O3 = Fe2(SO4)3 + 3H2O NaCl,Fe2(SO4)3
试题分析:(1)根据题意,小袋中装有铁粉、碳粉和少量氯化钠,故加入稀硫酸后,稀硫酸能与其中的铁粉反应,生成硫酸亚铁和氢气,故反应的化学方程式为Fe+H2SO4=FeSO4+H2↑。
(2)根据铁的锈蚀条件可知,“热宝”发热,其实是利用了铁粉与空气中的氧气和水反应放出的热量,故其失效后生成氧化铁,所以再加入一定量的稀硫酸能与之反应,生成硫酸铁和水,故反应的化学方程式3H2SO4 + Fe2O3 = Fe2(SO4)3 + 3H2O;则充分反应后过滤,则滤液中一定有的溶质是反应生成的Fe2(SO4)3和原袋中原有的少量氯化钠。
点评:在解此类方程式的书写题时,首先确定反应原理,然后再依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式。

练习册系列答案
相关题目
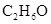 )具有清洁无污染的特点,将有望成为一种全新的替代能源。下列说法错误的是
)具有清洁无污染的特点,将有望成为一种全新的替代能源。下列说法错误的是  2P2O5
2P2O5