题目内容
我市北部山区盛产石灰石,石灰石的主要成分是碳酸钙。
(1)实验室中常用石灰石制取二氧化碳,化学的反应方程式为 ;
其中碳酸钙中钙元素的质量分数为 。
(2)某校课外活动小组为了解石灰石资源的品质,对当地石材进行化学分析:取12.5g石灰石颗粒样品,置于烧杯中并加入足量稀盐酸,充分反应后称得混合物的总质量减少4.4g。则该石灰石中含碳酸钙的质量分数是 。
(1)实验室中常用石灰石制取二氧化碳,化学的反应方程式为 ;
其中碳酸钙中钙元素的质量分数为 。
(2)某校课外活动小组为了解石灰石资源的品质,对当地石材进行化学分析:取12.5g石灰石颗粒样品,置于烧杯中并加入足量稀盐酸,充分反应后称得混合物的总质量减少4.4g。则该石灰石中含碳酸钙的质量分数是 。
(1)CaCO3 + 2HCl ="==" CaCl2 + H2O + CO2↑ 40% (2)80%
试题分析:(1)实验室中常用石灰石和稀盐酸反应制取二氧化碳,同时还生成了氯化钙和水,故反应的化学方程式为CaCO3 + 2HCl = CaCl2 + H2O + CO2↑;根据化合物中某元素的质量分数=
 ×100%可知,碳酸钙中钙元素的质量分数=
×100%可知,碳酸钙中钙元素的质量分数=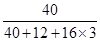 ×100%=40%。
×100%=40%。(2)根据题意,结合反应的化学方程式可知,充分反应后称得混合物的总质量减少,是因为反应中有二氧化碳气体生成并逸出,故减少的4.4g质量即为二氧化碳的质量;再利用化学方程式中碳酸钙与二氧化碳的质量比,可求出碳酸钙的质量,进而求出该石灰石中含碳酸钙的质量分数。
解,设该石灰石中含碳酸钙的质量为x
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
100 44
x 4.4g
100:44=x:4.4g
解得,x=10g
所以,该石灰石中含碳酸钙的质量分数=
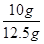 ×100%=80%。
×100%=80%。答:石灰石中含碳酸钙的质量分数为80%。
点评:本题为有关化学式的计算,以及根据化学方程式的计算,解题的关键是找出相关的化学反应,并根据质量守恒定律判断出生成二氧化碳的质量,然后依据已知量对未知的应求量进行求解计算即可,注意解题要规范

练习册系列答案
相关题目
 。
。