题目内容
【题目】下面是某化学兴趣小组的同学对氢氧化钠部分性质的探究过程:
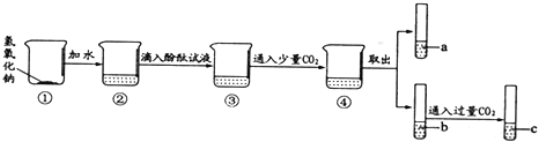
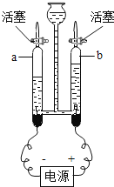
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会 (填“吸热”或“放热”),该溶液呈 色;③中的溶液显 色.
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈 性(填“酸”或“碱”).
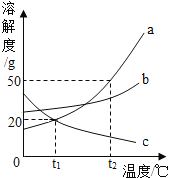
(3)c溶液和a溶液对比,c溶液颜色更浅.
【提出问题】
为什么继续通入过量的二氧化碳气体溶液颜色会更浅?
【设计实验】
实验操作 | 实验现象 | 实验结论 | |
甲 | 取少量c溶液滴入稀盐酸 | 有气泡产生 | 溶液中含较多的CO32﹣或HCO3﹣ |
乙 | 另取少量c溶液滴入硝酸钙溶液 | 无明显现象 | 溶液中没有大量的 离子 |
【实验结论】
根据甲、乙两个实验得出的结论,写出甲实验中发生反应的化学方程式: .
【实验反思】
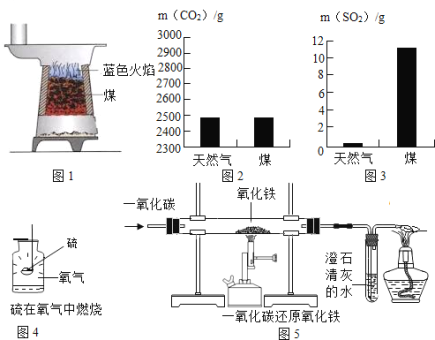
同种反应物在不同的条件下发生化学反应时,可能得到不同的产物.如:碳在氧气中燃烧可以生成 或 .
【答案】(1)放热;无;红;(2)碱性;(3)【设计实验】碳酸根;【实验结论NaHCO3+HCl=NaCl+H2O+CO2↑【实验反思】二氧化碳;一氧化碳;
【解析】
试题分析:(1)氢氧化钠固体溶解于水放热、溶液呈无色、氢氧化钠的溶液呈碱性,能使酚酞溶液变红;
(2)溶液颜色仍显红色,说明二氧化碳和氢氧化钠反应后的溶液仍然显碱性;
(3)【设计实验】加入硝酸钙无明显现象,说明溶液中不存在碳酸根离子,否则将产生白色沉淀;
【实验结论】根据实验得出结论溶液中的溶质为碳酸氢钠,方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑
【实验反思】很多物质在不同条件下会产生不同的产物,碳在氧气充足的时候生成二氧化碳,在氧气不足的时候生成一氧化碳;

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目