题目内容
酸、碱、盐是重要的化合物,它们之间能发生复分解反应。
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有 生成。
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量氢氧化钠溶液中,实验无明显现象。为确定反应后溶液中有哪些成分,同学们进行了实验探究。请填写下表:
| 实验操作 | 测定结果 | 溶液成分 |
| ①用pH试纸测定反应后溶液的酸碱度,操作方法是 。 | ②若pH>7 | |
| ③若 | NaCl |
(3)实验反思:无明显现象的中和反应可借助 判断反应终点。
(4)右边是某趣味实验装置图。挤压胶头滴管后,可观察到气球胀大的现象。请分析其原因,并写出化学方程式。

(5)某工厂利用铁屑与硫酸起反应来制取硫酸亚铁。现有稀硫酸49t,
与足量铁屑起反应,可生产7.6 t硫酸亚铁,试计算稀硫酸中溶质
的质量分数是多少?
(1)水;(2)①用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较;②NaCl、NaOH(或氯化钠、氢氧化钠);③pH=7
(3)酸碱指示剂(或答出具体的酸碱指示剂也可)(4)CO2被浓NaOH溶液吸收,锥形瓶内的气压成小,外界大气压大于锥形瓶内的气压,使气球胀大; 2NaOH + CO2 =Na2CO3 + H2O;(5)10%
解析试题分析:(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成;(2)①用pH试纸测定反应后溶液的酸碱度,操作方法是用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较;②若pH>7溶液成分为氯化钠和氢氧化钠;③若pH="7" ,溶液成分为氯化钠;(3)实验反思:无明显现象的中和反应可借助酸碱指示剂判断反映的终点;(4)挤压胶头滴管后,可观察到气球胀大的现象。其原因为CO2被浓NaOH溶液吸收,锥形瓶内的气压成小,外界大气压大于锥形瓶内的气压,使气球胀大;,化学方程式为2NaOH + CO2 =Na2CO3 + H2O
(5)解:设硫酸的质量分数为X。
Fe + H2SO4 = FeSO4 + H2↑
98 152
49t×X 7.6t
98:152 = 49 t×X :7.6 t
X = 10%
答:硫酸的质量分数10%。
考点:复分解反应的条件、中和反应、根据化学方程式的计算

某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验,向烧杯中的氢氧化钙溶液滴加一定量的稀盐酸后,发现忘记滴加指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中溶质的成分进行探究。
(1)写出该中和反应的化学方程式_______________________。
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】
(A)溶质可能是CaCl2与Ca(OH)2
(B)溶质可能是CaCl2
(C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。于是排除了猜想(A),你认为排除猜想(A)的理由是_____________。
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液 | | 猜想(B)正确 |
| | 猜想(C)正确 |
A.取反应后的溶液于试管中,滴加紫色石蕊试液变红色
B.取反应后的溶液于试管中,加入锌粉冒气泡
C.用洁净的玻璃棒蘸取反应后的溶液,涂抹在pH试纸上,测溶液的pH <7
D.取反应后的溶液于试管中,加入硝酸银溶液,生成白色沉淀
(8分)“海水晒盐”所获得的粗盐中,除含有泥沙等难溶性杂质外,还含有氯化镁、氯化钙等可溶性杂质,某化学小组为得到较纯净的食盐,进行了下列实验探究活动,请参与他们的探究活动。
[提出问题]如何获得较纯的食盐晶体?
[查阅资料]
20℃时,部分物质的溶解性
情况如下表所示:
| | OH- | CO32- |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
[实验方案]按如下方案进行提纯粗盐。

[解释与结论]
(1)实验操作X的名称是 ;沉淀D是 。
(2)为达到除去难溶性杂质的实验步骤是 。(填序号)
(3)实验步骤③的主要目的是 (用化学方程式回答);判断氢氧化钠溶液已过量的方法是 。
(4)在进行实验步骤⑤的蒸发时,为防止液体飞溅和获得相对更纯的食盐晶体需要进行的操作是 。
[反思与评价]
(5)有同学认为该实验方案并不完善,其理由及需补充的实验操作是 。
某化学学习小组的同学围绕“澄清石灰水与碳酸钠溶液的反应”展开了如下探究活动。
(1)该反应的化学方程式为_______________________________________。
(2)反应后溶液中的溶质是什么?同学们一致认为有以下三种情况:①氢氧化钠和氢氧化钙;②氢氧化钠和碳酸钠;③____________________________。
(3)小新取少量溶液于试管中,滴加过量稀盐酸,发现无气泡产生,说明情况________(填序号)是不可能的。
为了进一步确定溶液的成分,同学们设计了如下实验方案:
| 实验步骤 | 现 象 | 结 论 |
| | | 情况①正确 |
小红选择了另外一种不同类别的物质________________________________(填化学式),也得到了同样的结论。在同学们的合作下,他们顺利完成了探究任务。
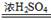 CO↑+ CO2↑+ H2O
CO↑+ CO2↑+ H2O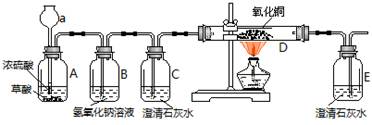
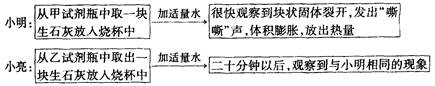

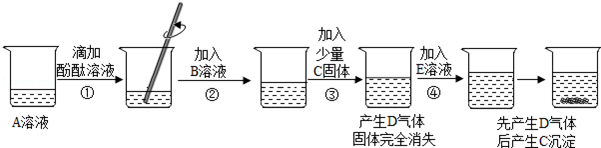 回答下列问题:
回答下列问题: