题目内容
【题目】如下图中的A~I是初中化学中常见的九种物质,是由C、H、O、Fe、Cu五种元素组成的单质或氧化物,其中C、F、H、I为氧化物,且C中氧元素的质量分数为20%;B、H为红色固体;通常D→B是在溶液中发生的反应。图中“—”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物或生成物已略去。
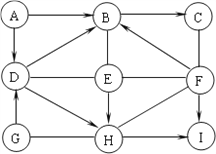
(1)H的化学式为__________。
(2)F—H反应的化学方程式为:___________,该反应的用途是___________。
(3)写出D→B的化学方程式_____________,该基本反应类型是____________。
【答案】 Fe2O3 3CO+Fe2O3![]() 2Fe+3CO2 (高炉)炼铁 Fe+CuSO4===Cu+FeSO4 置换反应(必须有反应二字)
2Fe+3CO2 (高炉)炼铁 Fe+CuSO4===Cu+FeSO4 置换反应(必须有反应二字)
【解析】A~I是初中化学常见的物质,是由C、H、O、Fe、Cu五种元素组成的单质或氧化物,其中C、F、H、I为氧化物,且C中氧元素的质量分数为20%;B、H为红色固体;通常D→B是在溶液中发生的反应,所以H是氧化铁,C是氧化铜,B是铜,所以D是铁,氧化铜会与F反应,F会转化成B,所以F是一氧化碳, A、G是碳或氢气,E是氧气,I是二氧化碳,经过验证,推导正确;(1) H是氧化铁,化学式为Fe2O3;(2)一氧化碳和氧化铁反应化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;此原理应用于炼铁;(3)铁在溶液中生成铜的化学方程式为:Fe+CuSO4=Cu+FeSO4;此反应属于置换反应。
2Fe+3CO2;此原理应用于炼铁;(3)铁在溶液中生成铜的化学方程式为:Fe+CuSO4=Cu+FeSO4;此反应属于置换反应。

【题目】硅钢是制变压器、充电器的核心材料,其主要成分是Fe和Si。某同学用硅钢样品进行如下实验:取6.60 g硅钢样品,将60.00 g稀硫酸分6次加入样品中(其中稀硫酸与硅及其他杂质不反应)。实验测得相关数据如下:
稀硫酸的用量 | 剩余固体的质量 |
第1次加入10.00 g | W g |
第2次加入10.00 g | 4.36 g |
第3次加入10.00 g | 3.24 g |
第4次加入10.00 g | 2.12 g |
第5次加入10.00 g | 1.00 g |
第6次加入10.00 g | 1.00 g |
(1)根据表中数据,稀硫酸加入到第________次,铁恰好反应完全。
(2)表中W=________g。
(3)计算该稀硫酸溶质的质量分数是__________(写出计算过程)。