题目内容
(10哈尔滨).53. (4分)如图所示,将蜡烛和装有碱石灰(主要成分为氧化钙和氢氧化钠的混合物)的玻璃管固定在已调平的天平左盘,往右盘加砝码至天平平衡。点燃蜡烛,使燃烧产物全部被碱石灰吸收。
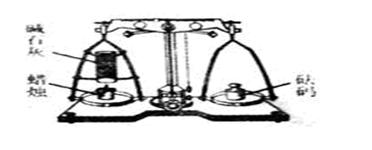
⑴蜡烛燃烧过程中,天平的(填“左”或“右”)盘_______逐渐下沉。
⑵根据质量守恒定律解释天平失去平衡的原因。

⑴蜡烛燃烧过程中,天平的(填“左”或“右”)盘_______逐渐下沉。
⑵根据质量守恒定律解释天平失去平衡的原因。
⑴左盘
⑵根据质量守恒定律,参加化学反应的物质的质量等于生成物的质量,反应物是蜡烛和空气中的氧气,生成物全部被碱石灰吸收,而原来的平衡左边是蜡烛和碱石灰,没包含参加反应的氧气的质量,所以左盘会下沉
⑵根据质量守恒定律,参加化学反应的物质的质量等于生成物的质量,反应物是蜡烛和空气中的氧气,生成物全部被碱石灰吸收,而原来的平衡左边是蜡烛和碱石灰,没包含参加反应的氧气的质量,所以左盘会下沉
本题考查的是质量守恒定律的实验探究,生石灰的性质与用途,碱的化学性质,质量守恒定律及其应用。蜡烛燃烧生成二氧化碳和水,碱石灰能够吸收二氧化碳和水,从理论上讲,可用于验证质量守恒定律,但是装置是开放的空间,生成的热的二氧化碳和水蒸气可能被碱石灰全部吸收,也可能有来不及吸收的气体逸出,所以此时天平就会失去平衡。因此若利用有气体参加或生成的反应验证质量守恒定律时,必须在密闭的容器内进行。由装置图可知,蜡烛和碱石灰处于开放的空间,燃烧生成的热的二氧化碳和水蒸气被碱石灰全部吸收,而先前并没有称量反应掉的氧气的质量,所以导致天平的左盘就会逐渐下沉。

练习册系列答案
相关题目


 (3)两种方案,你认为不能达到目的的是________(填“A”或“B”),理由是________。
(3)两种方案,你认为不能达到目的的是________(填“A”或“B”),理由是________。


