题目内容
下列试剂瓶标签上的化学式书写错误的是( )A.
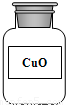
B.

C.

D.

【答案】分析:化合物中各元素或原子团的化合价的代数和为零.
金属的化学式用组成元素的元素符号来表示.
解答:解:根据标签上的化合物的化学式计算化合物中各元素的化合价的代数和:
氧化物中铜、氧元素的化合价分别为+2和-2,氧化铜中各元素的化合价的代数和为(+2)+(-2)=0;
硝酸钾中钾、硝酸根的化合价分别为+1和-1,硝酸钾中各元素或原子团的化合价的代数和为(+1)+(-1)=0;
氯化钙中钙、氯元素的化合价分别为+2和-1,氯化钙中各元素的化合价的代数和为(+2)+(-1)=+1≠0
锌是金属,其化学式为锌元素的元素符号Zn.
故选C.
点评:本题主要考查化学式的书写和意义,难度稍大.
金属的化学式用组成元素的元素符号来表示.
解答:解:根据标签上的化合物的化学式计算化合物中各元素的化合价的代数和:
氧化物中铜、氧元素的化合价分别为+2和-2,氧化铜中各元素的化合价的代数和为(+2)+(-2)=0;
硝酸钾中钾、硝酸根的化合价分别为+1和-1,硝酸钾中各元素或原子团的化合价的代数和为(+1)+(-1)=0;
氯化钙中钙、氯元素的化合价分别为+2和-1,氯化钙中各元素的化合价的代数和为(+2)+(-1)=+1≠0
锌是金属,其化学式为锌元素的元素符号Zn.
故选C.
点评:本题主要考查化学式的书写和意义,难度稍大.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案
相关题目
实验室有一保管不当的试剂瓶,其残缺的标签中只剩下“Na”字样.已知它是无色液体,是初中化学常用的无机试剂.小宏同学为探究其成份进行了猜想,并设计实验进行验证,有关内容见下表:
| 猜想 | 设计的实验步骤 | 可能的现象与结论 |
| 猜想一:可能是氢氧化钠溶液 | 用试管取少量样品,向其中滴入两滴酚酞试液. | 若酚酞试液变为红色,则猜想成立. 若酚酞试液无明显变化,则猜想不成立. |
| 猜想二:? | 用试管取少量样品,向其中先滴入适量的用硝酸酸化的硝酸钡溶液,然后滴入硝酸银溶液. | 若溶液先没有明显变化,后出现白色沉淀,则猜想成立.若与上述现象不同,则猜想不成立. |
| 猜想三:? | 用试管取少量样品,向其中先加入适量盐酸酸化,然后滴入氯化钡溶液. | 若溶液先没有明显变化,后出现白色沉淀,则猜想成立.若与上述现象不同,则猜想不成立. |
(1)小宏的猜想二是:______.
(2)小宏的猜想三是:______.如果猜想成立,则产生沉淀的化学反应方程式为:______.
(3)小宏同学对猜想一所描述的实验现象和作出的结论是否正确?请判断并说明理由. ______.
实验室有一保管不当的试剂瓶,其残缺的标签中只剩下“Na”字样.已知它是无色液体,是初中化学常用的无机试剂.小宏同学为探究其成分进行了猜想,并设计实验进行验证,有关内容见下表:
请你参与这一探究活动,根据上表回答下列问题:
(1)小宏的猜想二是:______.如果猜想成立,则产生沉淀的化学反应方程式为______.
(2)小宏的猜想三是:______.如果猜想成立,则产生沉 淀的化学反应方程式为______.
(3)小宏同学对猜想一所描述的实验现象和作出的结论是否正确?______,请说明理由______.
(4)除了小宏的三种猜想,请你再补充一种猜想,模仿上述过程,设计简单的实验方案并验证你的猜想,将有关内容填入下表.
| 猜想 | 设计的实验步骤 | 可能的现象与结论 |
| 猜想一:可能是氢氧化钠溶液 | 用试管取少量样品,向其中滴入两滴酚酞试液. | 若酚酞试液变为红色,则猜想成立. 若酚酞试液无明显变化,则猜想不成立. |
猜想二:? | 用试管取少量样品,向其中先滴入适量的稀硝酸,然后滴入硝酸银溶液. | 若溶液先没有明显变化,后出现白色沉淀,则猜想成立.若与上述现象不同,则猜想不成立. |
猜想三:? | 用试管取少量样品,向其中先加入适量盐酸酸化,然后滴入氯化钡溶液. | 若溶液先没有明显变化,后出现白色沉淀,则猜想成立.若与上述现象不同,则猜想不成立. |
(1)小宏的猜想二是:______.如果猜想成立,则产生沉淀的化学反应方程式为______.
(2)小宏的猜想三是:______.如果猜想成立,则产生沉 淀的化学反应方程式为______.
(3)小宏同学对猜想一所描述的实验现象和作出的结论是否正确?______,请说明理由______.
(4)除了小宏的三种猜想,请你再补充一种猜想,模仿上述过程,设计简单的实验方案并验证你的猜想,将有关内容填入下表.
| 你补充的猜想 | 设计的实验步骤 | 可能的现象与结论 |
| ______ | ______ | ______ |