题目内容
【题目】以下是某研究小组探究影响反应速率部分因素的相关实验数据。
实验序号 | 过氧化氢溶解浓度/% | 过氧化氢 溶解液体积 | 温度/℃ | 二氧化锰的用量/g | 收集氧气体积mL | 反应所需 的时间 |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | / | 2 | 49.21 |
④ | 30 | 5 | 55 | / | 2 | 10.76 |
(1)通过实验①②对比可知,化学反应速率与_____有关;
(2)通过实验_____(填两个实验序号)对比可知,化学反应速率与温度的关系是_____;
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量_____(选填“减小”、“不变”或“增大”)。
(4)写出此反应的文字表达式_____。
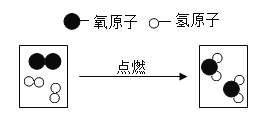
【答案】反应物的浓度 ③④ 温度越高,化学反应速率越快 不变 过氧化氢![]() 水+氧气
水+氧气
【解析】
(1)从表中分析可知:①②是过氧化氢浓度不同而其他的反应时各种量均相同,可知这一过程是考查反应物的浓度与反应速度的关系;故填:反应物的浓度;
(2)③④则是温度不同其他条件相同,明显是对温度影响化学反应速度的探究,由实验数据可知,化学反应速率与温度的关系是温度越高,化学反应速率越快;故填:③④;温度越高,化学反应速率越快;
(3)过氧化氢的浓度虽然改变,但反应物过氧化氢的量并未增减,因此生成氧气的量不变;故填:不变;
(4)过氧化氢在二氧化锰的催化作用下分解为水和氧气;故填:过氧化氢![]() 水+氧气。
水+氧气。

【题目】我国现有人口约14亿,水资源总量约为2.8×1012m3,水的紧缺程度与人均水量的关系如下:
人均水量/m3 | 小于500 | 500﹣1000 | 1000﹣1700 | 1700﹣3000 |
紧缺程度 | 极度缺水 | 严重缺水 | 中度缺水 | 轻度缺水 |
(1)根据计算我国的人均水量判定我国的水资源紧缺程度为_____;
(2)水资源的短缺很大一部分原因是由于水体受到污染,有关部门用大量活性炭来净化水质,这是利用了活性炭的_____性,此种方法净化后得到的水属_____。(填“纯净物”或“混合物”)
(3)为保护有限的水资源,请说出生活中的一点节约用水或防止水污染的具体做法:_____