题目内容
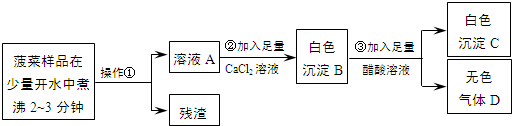
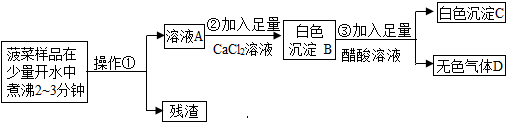
草酸钙(Ca C2O4)是不能被人体吸收的沉淀物,豆腐中含有较多的钙盐【硫酸钙(CaSO4)等】,波菜、洋葱、竹笋中含有丰富的草酸(H2C2O4),草酸钠(Na2 C2O4)。豆腐和上述几种蔬菜混合食用,可能诱发“结石症”。
(1)由草酸的化学式可知,其中碳元素的化合价是____。
(2)草酸与硫酸钙反应的化学方程式为:H2C2O4+ CaSO4= Ca C2O4↓+ H2 SO4,
请写出草酸钠与硫酸钙反应生成草酸钙和硫酸钠(Na2 SO4)的化学方程式: _________________。
【答案】
(1)+3
(2)Na2 C2O4+ CaSO4= Ca C2O4↓+ Na2 SO4
【解析】
试题分析:(1)化合价的规则:在化合物中,所有元素的化合价正负的代数和为零。而单质中,元素的化合价为零,常见元素化合价口诀:一价钾钠氯氢银,二价钙镁氧钡锌,二四六硫二四碳,三铝四硅五价磷, 铁有二三要分清,莫忘单质都是零.在H2C2O4中H的化合价为+1,O的化合价为-2,故可设C的化合价为x,则+1×2+x×2+(-2)×4=0,算出x=+3
(2)根据草酸与硫酸钙反应的化学方程式为:H2C2O4+ CaSO4= Ca C2O4↓+ H2 SO4,可知是按复分解反应类型进行,所以草酸钠与硫酸钙反应生成草酸钙和硫酸钠(Na2 SO4)的化学方程式:Na2 C2O4+ CaSO4= Ca C2O4↓+ Na2 SO4
考点:化合价的一般规律,化学方程式的书写

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目