题目内容
【题目】如图中的![]() 、
、![]() 是钼元素的部分信息,A、B、C、D是四种粒子的结构示意图
是钼元素的部分信息,A、B、C、D是四种粒子的结构示意图![]() 请回答下列问题:
请回答下列问题:
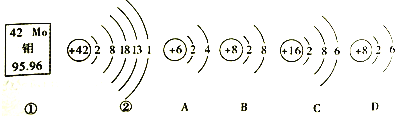
(1)钼元素的相对原子质量为______,该原子核内质子数是______.
(2)钼元素的原子易______(填“得”或“失”)电子.
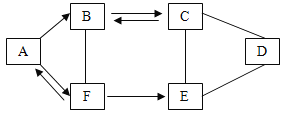
(3)A、B、C、D四种粒子中属于同种元素的是______![]() 填序号
填序号![]() .
.
(4)请写出Na元素与图中C元素组成的化合物的化学式______.
【答案】95.96 42 失 BD ![]()
【解析】
(1)图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量;原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层;
![]() 若最外层电子数
若最外层电子数![]() ,在化学反应中易得电子,若最外层电子数
,在化学反应中易得电子,若最外层电子数![]() ,在化学反应中易失去电子;
,在化学反应中易失去电子;
![]() 元素的种类与原子的核内质子数有关,据此解答即可;
元素的种类与原子的核内质子数有关,据此解答即可;
![]() 根据化合物化学式的写法分析解答。
根据化合物化学式的写法分析解答。
(1)根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,钼元素的相对原子质量为95.96,原子序数为42,原子序数![]() 质子数=42,该原子核内质子数是42;
质子数=42,该原子核内质子数是42;
(2)由钼原子的结构示意图可知:最外层弧线上的数字是1,最外电子层上有1个电子,在化学反应中易失去1个电子而形成阳离子;
(3)元素的种类与原子的核内质子数有关,A、B、C、D四种粒子中BD的原子核内的质子数相等,属于同种元素;
(4)据图可知C是硫元素,钠元素和硫元素可以组成硫化钠,化学式为:![]() 。
。

 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案【题目】完成下列探究实验.
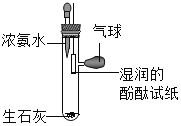
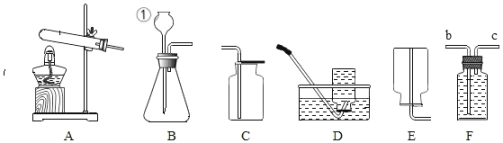
(1)小然同学设计探究分子运动的实验如图1,请按要求完成下列各小题:
①滴入适量浓氨水后,观察到酚酞试纸__________,原因是____.
②放入少量生石灰的作用是____,试写出发生的化学反应方程式____.
(2)有一袋白色粉末,甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠;丁同学认为是碳酸钠和碳酸氢钠的混合物.为了探究该白色粉末的成分,进行了以下实验:
①将少量白色粉末放入水中搅拌,观察到____,说明甲同学的猜想不正确.
②室温时,分别向盛有等质量的碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%的盐酸,记录如下表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
名称 | 质量/g | ||
Ⅰ | 碳酸氢钠 | 0.10 | V1 |
Ⅱ | 碳酸钠 | 0.10 | V2 |
Ⅲ | 白色粉末 | 0.10 | V3 |
(解释与结论)
③实验I的化学方程式为_____;
④表中V1___V2(填“>”、“<”或“=”);
⑤若V1>V3>V2则白色粉末物质为_____