题目内容
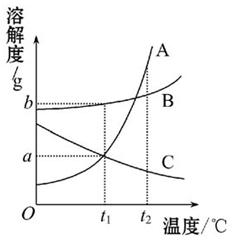
如图为KNO3和NaCl两种物质的溶解度曲线。

(1)两种物质的溶解度受温度的影响变化较大的是 (填KNO3或NaCl)。
(2)t1℃时,两种物质溶解度的大小关系为KNO3 NaCl。(填“>”、“=”、“<”)
(3)t2℃时,将25g KNO3固体投入50g水中,充分溶解后,所得溶液中溶质的质量分数为 。

(1)两种物质的溶解度受温度的影响变化较大的是 (填KNO3或NaCl)。
(2)t1℃时,两种物质溶解度的大小关系为KNO3 NaCl。(填“>”、“=”、“<”)
(3)t2℃时,将25g KNO3固体投入50g水中,充分溶解后,所得溶液中溶质的质量分数为 。
(1)KNO3 (2)< (3)33.3%(1/3)
试题分析:溶解度曲线意义:1、表示某物质在不同温度下的溶解度或溶解度随温度变化的情况,进而判断结晶的方法,①溶解度随温度的升高而增大,采用冷却热饱和溶液(即降温结晶),②溶解度随温度的升高而变化不大,采用蒸发结晶,2、两曲线的交点表示两种溶质在同一温度下具有相同的溶解度,3、可比较同温下,不同物质溶解度的大小关系,4、可直接读出某温下,物质的溶解度
(1)据图可知两种物质的溶解度受温度的影响变化较大的是KNO3
(2)t1℃时,两种物质溶解度的大小关系为KNO3<NaCl
(3)t2℃时,KNO3的溶解度为50g,所以将25g KNO3固体投入50g水中,能够全部溶解,刚好形成饱和溶液,所以所得溶液中溶质的质量分数=25g/75g×100%=33.3%

练习册系列答案
相关题目