题目内容
【题目】请阅读下列叙述后。回答问题。
小葵查询相关资料后,知道要配制某种浓度的NaOH水溶液100mL,需加入NaOH 16.0g。如图的步骤一至步骤四为她在室温下进行此浓度溶液配制,以及溶液密度测量的步骤示意图。步骤四完成后,经老师提醒,才知道烧杯上的刻度标示仅为参考之用,误差较大。所以小葵待溶液温度回到室温后,再以量筒测量溶液的总体积如步骤五所示。

依测量的结果可知,用此方法和器材配制溶液确实会有较大的误差。应改用容量瓶等器材来配制溶液。小葵原本想配制的溶液体积摩尔浓度,以及实际配制出的浓度依序为何?(H、O和Na的原子量分别为1、16和23)
A.0.4M、小于0.4MB.0.4M、大于0.4M
C.4.0M、小于4.0MD.4.0M、大于4.0M
【答案】D
【解析】
16.0g氢氧化钠物质的量:![]() =0.4mol,小葵原本想配制的溶液体积摩尔浓度:
=0.4mol,小葵原本想配制的溶液体积摩尔浓度: ![]() =4mol/L,实际溶液体积是0.095L,实际配制出的浓度:
=4mol/L,实际溶液体积是0.095L,实际配制出的浓度:![]()
![]() 4.2mol/L,因此小葵原本想配制的溶液体积摩尔浓度,以及实际配制出的浓度依序为4.0M、大于4.0M。
4.2mol/L,因此小葵原本想配制的溶液体积摩尔浓度,以及实际配制出的浓度依序为4.0M、大于4.0M。
故选:D。

【题目】实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小欣和小芳同学很感兴趣,决定对其成分进行探究:
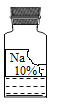
(1)根据受损标签的情况判断,这瓶试剂不可能是_____(填字母代号)。
A 酸 B 碱 C 盐
(2)Ⅰ.实验员说,这瓶试剂可能是NaCl、NaOH、Na2CO3、NaHCO3,并提示:Na2CO3、 NaHCO3的水溶液均显碱性。
Ⅱ.查阅资料:室温(20℃)时,四种物质的溶解度的数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
(得出结论)
小欣根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是_____,有同学再次认真观察排除,该同学认为不可能是_____。
(设计并实验)
请你设计实验确定这瓶试剂的名称,并完成以下实验报告。
(实验室仅提供了酚酞、稀盐酸、氢氧化钙溶液以及常用的实验仪器)
实验步骤 | 实验现象与结论 |
_____ | _____ |