题目内容
【题目】某化学兴趣小组的同学对实验室制取CO2及相关性质进行一系列的探究活动.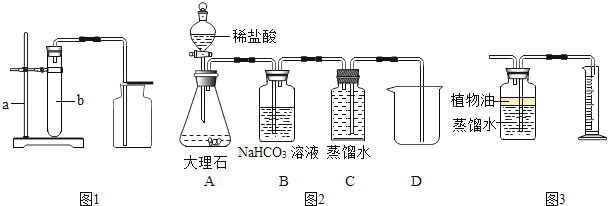
(1)气体制取.按如图甲所示的制取装置进行实验.
①写出有标号仪器的名称:a , b .
②实验室制取CO2的反应化学方程式是 ;
③实验室制取CO2的方法是 .原因是 .
(2)实验探究.
[提出问题]实验室制取CO2的时能否采用排水法收集?
[设计实验]实验一:向一个充满CO2气体的质地较软的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,用力摇晃塑料瓶.
可观察到塑料瓶 . 说明CO2能溶于水.
实验二:先用集气瓶装满一瓶蒸馏水(pH=7.0).然后按如图乙所示组装装置并进行实验,再用pH计测定从装置C排到烧杯中的液体的pH.
①装置B中碳酸氢钠溶液的作用是 .
②测得烧杯中液体的PH<7.0,说明溶液呈酸性,原因是: .
[实验结论]实验室制取CO2不宜采用排水法收集.
[拓展延伸]某同学先先对图乙装置做了以下改进:将装置C中的部分蒸馏水换成植物油,将烧杯换成量筒(如图丙所示).然后利用改进后的装置测定收集到CO2的体积,测得气体的实际体积小于理论值,原因可能是:① ;② .(合理即可)
【答案】
(1)铁架台;大试管;CaCO3+2HCl=CaCl2+H2O+CO2↑;用稀盐酸和大理石或石灰石反应制取CO2;用稀盐酸和大理石或石灰石反应,速率适中容易控制,大理石的来源广,所得CO2气流平稳,气体又较为纯净,所以选用稀盐酸制CO2
(2)变瘪;吸收二氧化碳气体中混杂的氯化氢气体;二氧化碳溶于水生成碳酸,使溶液呈酸性;二氧化碳被装置B中碳酸氢钠溶液少量吸收;量筒读数时视线偏低(或仰视)
【解析】(1)铁架台是常用的夹持仪器,大试管是常用的反应容器;实验室制取CO2 , 是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;用此法制二氧化碳的原因是:用稀盐酸和大理石或石灰石反应,速率适中容易控制,大理石的来源广,所得CO2气流平稳,气体又较为纯净,所以选用稀盐酸制CO2;故答案为:①铁架台;大试管;②CaCO3+2HCl=CaCl2+H2O+CO2↑;③用稀盐酸和大理石或石灰石反应制取CO2;用稀盐酸和大理石或石灰石反应,速率适中容易控制,大理石的来源广,所得CO2气流平稳,气体又较为纯净,所以选用稀盐酸制CO2;
(2)实验一:向一个充满CO2气体的质地较软的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,用力摇晃塑料瓶,可观察到塑料瓶变瘪,说明CO2能溶于水;故答案为:变瘪;
实 验二:实验二中,装置B中碳酸氢钠溶液的作用是:吸收二氧化碳气体中混杂的氯化氢气体;测得烧杯中液体的PH<7.0,说明溶液呈酸性,原因是:二氧化碳溶于水生成碳酸,使溶液呈酸性;故答案为:①吸收二氧化碳气体中混杂的氯化氢气体;②二氧化碳溶于水生成碳酸,使溶液呈酸性;
[拓展延伸]利用改进后的装置测定收集到CO2的体积,测得气体的实际体积小于理论值,原因可能是:二氧化碳被装置B中碳酸氢钠溶液少量吸收;量筒读数时视线偏低或仰视;故答案为:①二氧化碳被装置B中碳酸氢钠溶液少量吸收;②量筒读数时视线偏低(或仰视).
铁架台是常用的夹持仪器,大试管是常用的反应容器;制取装置包括加热和不需加热两种,实验室制取CO2 , 是在常温 下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此 只能用向上排空气法收集.原因是:用稀盐酸和大理石或石灰石反应,速率适中容易控制,大理石的来源广,所得CO2气流平稳,气体又较为纯净,所以选用稀盐酸制CO2;向一个充满CO2气体的质地较软的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,用力摇晃塑料瓶,可观察到塑料瓶变瘪,说明CO2能溶于水.
实验二中,装置B中碳酸氢钠溶液的作用是:吸收二氧化碳气体中混杂的氯化氢气体;测得烧杯中液体的PH<7.0,说明溶液呈酸性,原因是:二氧化碳溶于水生成碳酸,使溶液呈酸性;利用改进后的装置测定收集到CO2的体积,测得气体的实际体积小于理论值,原因可能是:二氧化碳被装置B中碳酸氢钠溶液少量吸收;量筒读数时视线偏低或仰视.

 快捷英语周周练系列答案
快捷英语周周练系列答案