题目内容
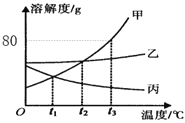
【题目】已知a、b、c三种物质的溶解度曲线如图所示,请回答下列问题:
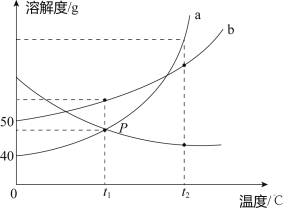
(1)欲使a、c饱和溶液同时析出晶体,可采用的方法是____________.
(2)将t2℃时的a、b、c三种物质的饱和溶液同时降温到t1℃,析出晶体最多的是___________(填“a”、“b”、“c”或“无法确定”,下同),所得溶液中溶质质量分数最小的是__________.
(3)t1℃时,在盛有50g水的三个烧杯中分别加入25g的a、b、c,然后将温度升温至t2℃(忽略水分的蒸发),下列关于a、b、c三种溶液说法正确的是__________(填字母).
A.a溶液中溶质质量不变
B.c溶液中一定有固体析出
C.b溶液为饱和溶液
D.溶液的溶质质量分数大小关系:a=b>c
【答案】蒸发溶剂 无法确定 c ABD
【解析】
(1)a物质的溶解度随温度的升高而增大,c物质的溶解度随温度的升高而减小,所以欲使a、c饱和溶液同时析出晶体,可采用的方法是蒸发溶剂;
(2)将t2℃时的a、b、c三种物质的饱和溶液同时降温到t1℃,a、b、c饱和溶液的质量不能确定,所以析出晶体最多的是无法确定;降温后会形成a、b在t1℃时饱和溶液,而c的溶解度随温度降低而增大,故c形成不饱和溶液,c的溶质质量分数不变,一定温度下饱和溶液的溶质质量分数=![]() ×100%,c在t2℃时的溶解度小于a和b在t1℃时的溶解度,故降温后所得溶液中溶质质量分数最小的是c;
×100%,c在t2℃时的溶解度小于a和b在t1℃时的溶解度,故降温后所得溶液中溶质质量分数最小的是c;
(3)t1℃时,在盛有50g水的三个烧杯中分别加入25g的a、b、c,t1℃时,a、c物质的溶解度是50g,b物质的溶解度大于50g,全部溶解;然后将温度升温至t2℃,t2℃时,a、b物质的溶解度都大于50g,a、b物质全部溶解,c物质的溶解度小于50g,没有全部溶解,因此:A、a物质的溶解度增大,a溶液中溶质质量不变,故A正确;B、c物质的溶解度随温度的升高而减小,所以c溶液中一定有固体析出,故B正确;C、b物质的溶解度增大,所以b溶液为不饱和溶液,故C错误;D、t2℃时,a、b物质的溶解度都大于50g,a、b物质全部溶解,c物质的溶解度小于50g,没有全部溶解。a、b溶液的溶质、溶剂质量相等,溶液的溶质质量分数相等,c没有全部溶解,溶液的溶质质量分数小于a、b,所以溶液的溶质质量分数大小关系:a=b>c,故D正确。故选ABD。

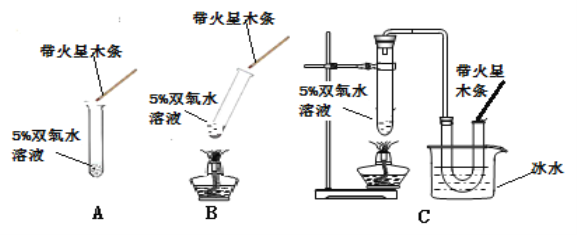
【题目】某化学兴趣小组同学在整理实验室药品时发现一瓶未盖好盖子的氢氧化钠固体,为了探究此氧氢氧化钠固体是否变质,同学们进行了有关实验.请你与他们一起完成以下探究活动:
(知识回顾)氢氧化钠变质的化学方程式为______________.
(假设猜想)假设一:氧氧化钠没有变质 假设二:氢氧化钠变质了
(实验探究)同学们设计了多种方法进行验证.
操作 | 现象 | 结论 | |
方法一 | 取该样品少量于试管里,加入适量的水,振荡,样品全部溶于水,再向其中滴加酚酞试液 | 溶液变红色 | 样品变质了 |
方法二 | 取该样品少量于试管里,加入足量稀盐酸 | 有气泡产生 | 样品变质了 |
方法三 | 取该样口少量于试管里,加入适量的水,振荡,样品全部溶于水,再加入足量的氯化钙溶液 | 溶液变浑浊 | 样品变质了 |
(得出结论)氢氧化钠变质了
(讨论交流)经过讨论,同学们一致认为只有方法____________的探究过程是严密的.另外两种方法探究过程出错的原因是____________(任选一种方法进行解释).
(拓展迁移)
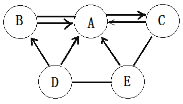
(1)同学们继续研究氢氧化钠固体是部分变质还是全部变质,过程如下:

A溶液中的溶质为___________;现象B是__________.
(2)为了将部分变质的氢氧化钠固体中的杂质除去,同学们做了如下实验:取固体加水溶解,向溶液中加入适量的_____________溶液,过滤后蒸发,即可得到纯净的氢氧化钠固体.
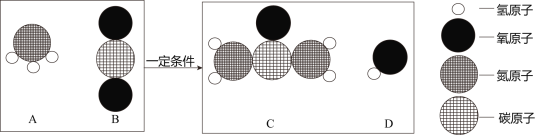
【题目】化学用语是学好化学的重要工具。
(1)按要求写出对应的化学符号(“![]() ”表示氮原子)。
”表示氮原子)。
|
| |
化学符号 | _______ | _______ |
(2)写出下列物质化学式。
名 称 | 氢氧化钙 | 硝酸银 | 硫酸铜 | 碳酸钾 |
化学式 | _____ | _____ | _____ | _____ |
名 称 | 氯化亚铁 | 硫酸 | 氧化铝 | 氢氧化镁 |
化学式 | _____ | _____ | _____ | _____ |