题目内容
【题目】向含10g NaOH的溶液中通入一定量的CO2,然后在低压条件下蒸干得12.6g白色固体,通过计算确定该白色固体的成分及其各组成成分的质量(写出计算过程).
[查阅资料]1、Na2CO3+CO2+H2O═2NaHCO3
2、NaHCO3溶液在低压蒸干条件下得到的固体不分解.
【答案】白色固体的成分是氢氧化钠和碳酸钠,质量分别是:2g、10.6g。
【解析】
试题分析:设10gNaOH与二氧化碳反应生成的碳酸钠的质量为x
CO2+2NaOH═Na2CO3+H2O.
80 106
10g x
![]() 解得:x=13.25g
解得:x=13.25g
由于12.6g小于13.6g,所以该白色固体的成分是氢氧化钠和碳酸钠.
设参加反应的氢氧化钠的质量为z,则生成的碳酸钠的质量为:12.6g﹣(10g﹣z)=2.6g+z
CO2+2NaOH═Na2CO3+H2O
80 106
z 2.6g+z
![]() 解得:z=8g
解得:z=8g
剩余的氢氧化钠的质量:10g﹣8g=2g,生成的碳酸钠的质量为:2.6g+8g=10.6g

练习册系列答案
相关题目
【题目】根据如图中的实验装置,回答问题:
发生装置 | 收集装置 | 洗气装置 |
|
|
|
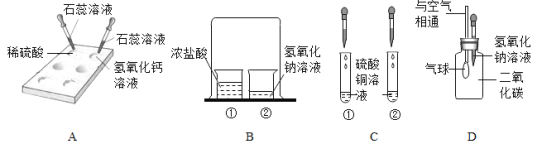
(1)写出图B中仪器a的名称: 。
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为 ,发生和收集装置为 (填字母)。
(3)实验室用石灰石和稀盐酸反应制取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的 端口(填“①”或“②”)通入,F中发生的化学方程式为 。