题目内容
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图:
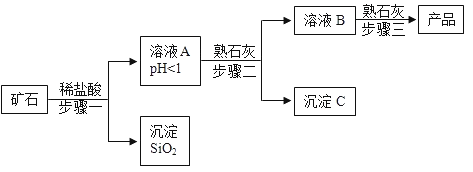
(1)请写出步骤一中发生反应的化学方程式: (任写一个)
(2)溶液A中所含的阳离子有 (填离子符号)
(3)已知:部分金属阳离子以氢氧化物形成沉淀时溶液的pH见表
沉淀物 | Fe(OH)2 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
步骤二中加入熟石灰,调节溶液的pH范围为
(4)3个步骤中均用到的操作是
(5)步骤三中生成产品的化学方程式为 .
【答案】(1)MgO+2HCl═MgCl2+H2O
(2)Mg2+、Fe3+、Cu2+、H+
(3)6.7~9.1
(4)过滤
(5)MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2
【解析】
试题分析:(1)矿石中含有MgO、Fe2O3、CuO这几种金属氧化物,都能与酸反应,故步骤一中发生反应的化学方程式为:MgO+2HCl═MgCl2+H2O
(2)溶液A是MgO、Fe2O3、CuO这三种金属氧化物与酸反应所得,且溶液pH<7,说明盐酸过量,故溶液中所含的阳离子有Mg2+、Fe3+、Cu2+、H+
(3)步骤二中加入熟石灰的目的是将溶液中的Fe3+、Cu2+沉淀完,使溶液中只剩下Mg2+,这样最后沉淀才能得到纯净的Mg(OH)2,所以根据表中的部分金属阳离子以氢氧化物形成沉淀时溶液的pH,故调节溶液的pH范围为6.7~9.1
(4)3个步骤中都要将沉淀与溶液分离,故均用到的操作是过滤
(5)步骤三中生成产品的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目