题目内容
【题目】硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,某同学设计了下列两条途径由废铜料(含铁)生产硫酸铜晶体,其过程如下所示:
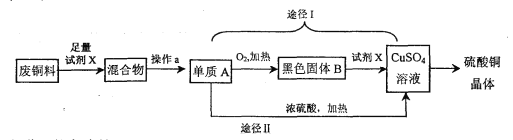
(1)操作a的名称是: ;
(2)已知:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。则途径I与途径II相比,其优点体现在:
①不产生二氧化硫有毒气体,不会污染空气;② ;
(3)将废铜料投入硫酸铜溶液中充分搅拌,发生反应的化学方程式为: 。
【答案】(1)过滤;
(2)硫酸根全部转化为硫酸铜,硫酸的利用率高;
(3)Fe + CuSO4== Cu + FeSO4。
【解析】
试题分析:(1)A可与浓硫酸在加热的情况下反应生成硫酸铜;所以A中一定含铜元素。又知A为单质,所以A为铜;则B为氧化铜;试剂X则为稀硫酸;废铜料的成分为铜铁混合物,铁与加入的硫酸反应生成硫酸亚铁(可溶);铜不反应。所以操作a将混合物中的固体与液体分离,应为过滤;
(2)途径I中的硫酸根全部转化为硫酸铜,硫酸的利用率高;而途径II中的硫酸根有一部分转化为二氧化硫,造成了资源的浪费。
(3)废铜料中的铁会与投入硫酸铜溶液发生置换反应,化学方程式为:Fe + CuSO4== Cu + FeSO4。

练习册系列答案
相关题目