题目内容
【题目】煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源,煤气化和液化流程示意图如下:
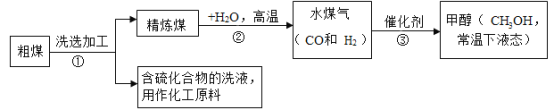
(1)第①步操作发生的是_____(填“物理”或“化学”)变化.
(2)第②步是精炼煤与水蒸气的反应,化学方程式为_____.
(3)第③步中参加反应的CO与H2的微粒个数比是1:2,该反应的基本类型属于_____,甲醇属于_____(填无机物或有机物).
(4)含硫化合物洗液经过提炼后,可用来制硫酸,过程是:含硫化合物氧化得到SO2,SO2进一步氧化得到X,X与水反应得到H2SO4,则X的化学式为_____.
(5)从“绿色化学”的角度分析,“煤的汽化和煤的液化”生产流程的优点_____.
【答案】物理 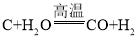 化合反应 有机物 SO3 原料全部转化为产品或实现“零排放”,不对环境造成污染
化合反应 有机物 SO3 原料全部转化为产品或实现“零排放”,不对环境造成污染
【解析】
(1)第①步操作是通过水流的冲击作用,把不同成分不同比重的原煤分出不同等级,并除去尘土和废石,降低灰分和硫分含量,并没有生成新物质,所以属于物理变化;故填:物理;
(2)第②步是煤与水蒸气在高温的条件下反应,生成氢气和一氧化碳,该反应的化学方程式为: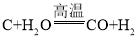 ;
;
(3)参加反应的CO与H2的微粒个数比是1:2,生成物是甲醇,因此,该反应的化学方程式为: ,该反应符合“一变多”的特点,属于化合反应;
,该反应符合“一变多”的特点,属于化合反应;
甲醇是一种含碳元素的化合物,属于有机物;
(4)SO2进一步氧化得到X,X与水反应得到H2SO4,则X是三氧化硫,三氧化硫的化学式为SO3,故填:SO3;
(5)从“绿色化学”的角度分析,“煤的气化和煤的液化”生产流程的优点是:原料全部转化为产品或实现“零排放”,不对环境造成污染;故填:原料全部转化为产品或实现“零排放”,不对环境造成污染。

练习册系列答案
相关题目