题目内容
【题目】根据“粗盐中难溶性杂质的去除”实验,回答有关问题。
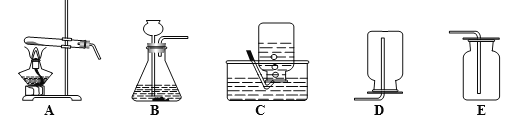
Ⅰ(1)实验步骤:
①溶解 称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.2g。
②过滤
③蒸发 请从溶解度的角度分析,试验中不采用降低溶液温度的方法得到精盐的依据是__________。
④计算产率 得到精盐3.2g,则精盐的产率为__________(计算结果保留一位小数)。
(2)整个实验中至少要进行__________次称量。
(3)从海水中获得的粗盐,经过上述实验得到的精盐属于__________(填“混合物”或“纯净物”)。
Ⅱ乙同学用天平称量一定量的可能含氯化镁、硫酸钠和氯化钙的粗盐,并设计了如下过程进行除杂提纯,实验后得到较纯净的氯化钠固体。(此题中微溶物视为可溶物)
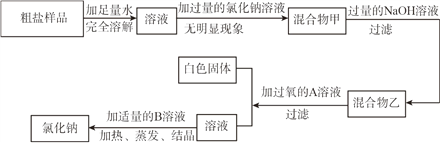
(1)混合物甲中一定有的成分是____________________。
(2)白色固体中一定有的成分为____________________。
(3)加入B溶液后的现象为____________________。
【答案】 氯化钠的溶解度受温度影响小 84.2% 3 混合物 NaCl,BaCl2,MgCl2 BaCO3 开始无现象,一段时间后产生气泡
【解析】Ⅰ(1)③从溶解度的角度分析,实验中不采用降低溶液温度的方法得到精盐的依据是:氯化钠的溶解度受温度的变化影响较小,相同情况下降温析出的晶体比较少;
故填:氯化钠的溶解度受温度的变化影响较小;
④精盐的产率为: ![]() =84.2%,
=84.2%,
(2)需要称量的数据有:最初所取粗盐的质量、剩余粗盐的质量(以此运用差量法得出溶解的粗盐的质量),以及所得精盐的质量,因此,最少需要3次称量;
(3)精盐中除了食盐,还有可溶性杂质,所以得到的精盐属于混合物;
Ⅱ(1)加入氯化钡溶液无明显现象,说明样品中不含有硫酸钠,加入氢氧化钠溶液后产生沉淀,说明样品中含有氯化镁,因此混合物甲中一定有的成分是氯化钠、氯化钡、氯化镁;
(2)加入碳酸钠溶液后得到的白色沉淀中一定有氯化钡和碳酸钠反应生成的碳酸钡,可能含有氯化钙和碳酸钠反应生成的碳酸钙,因此白色固体中一定有的成分为碳酸钡;
(3)加入的B溶液是稀盐酸,稀盐酸能和氢氧化钠反应生成氯化钠和水,能和碳酸钠反应生成氯化钠、水和二氧化碳,能够观察到开始无明显现象,后产生气泡。