题目内容
【题目】夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等。现在市场上出售一种称作“污渍爆炸盐”的商品,宜称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多顽固污渍”。小红同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化成分进行探究。
主要探究过程如下:
(1)提出问题“污渍爆炸盐”的主要化学成分是什么?
(2)查阅相关资料(资料主要信息如下)
过碳酸钠俗称固体双氧水,白色结晶颗粒。过碳酸钠溶与水反应时分解生成碳酸钠和过氧化氢,是目前广泛应用的主要洗涤助剂之一。
(3)猜想:“污渍爆炸盐”的主要化学成分可能是过碳酸钠。
(4)设计与实险
小红同学设计的主要实验装置如图所示。
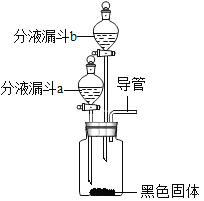
请你运用所学知识,助小红同学完成下列实验报告。
序号 | 主要操作步骤 | 主要实验现象 | 操作目的 |
① | 在集气瓶中加入少量______(黑色固体);在分液漏斗a中加入新配制的“污渍爆炸盐”的饱和溶液;在分液漏斗b中加入_______________。 | ||
② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞 | 生成大量无色气体 | |
然后________________ | _____________________ | 验证生成气体的成分 | |
第②步操作得到的结论:____________________。 | |||
③ | 待第②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞 | 生成大量无色气体 | |
将生成的气体通入_____________________ | ________________________________ | 验证生成气体的成分 | |
第③步操作得到的结论:_______________________。 | |||
(5)实验的初步结论
小红认为:“污渍爆炸盐”溶于水生成碳酸钠和过氧化氢,“污渍爆炸盐”的主要化学成分是过碳酸钠。
【答案】二氧化锰 稀盐酸溶液 用带火星的木条放在a瓶口 木条复燃 证明污渍爆炸盐溶于水可以生成过氧化氢 澄清石灰水 石灰水变浑浊 污渍爆炸盐溶于水可以生成碳酸钠
【解析】
本实验主要是通过验证过碳酸钠分解的产物来证明是否是这种物质.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,碳酸钠能和盐酸反应生成二氧化碳气体,过氧化氢遇二氧化锰能分解生成氧气,验证生成物中有氧气和二氧化碳生成,可证明该物质是过碳酸钠。
①.过氧化氢遇二氧化锰能分解生成氧气,故在集气瓶中加入少量的二氧化锰;
在分液漏斗b中加入稀盐酸溶液,可以与碳酸钠反应释放出二氧化碳;
②.打开分液漏斗a的活塞,放出适量溶液后,关闭活塞,过氧化氢在二氧化锰催化下生成氧气,故用带火星的木条放在a瓶口,木条复燃,说明产生的大量气体是氧气;
得出的结论是证明污渍爆炸盐溶于水可以生成过氧化氢;
③.待第②步反应停止后,打开分液漏斗b的活塞,放出适量的稀盐酸溶液后,关闭活塞,产生大量的二氧化碳气体;
将二氧化碳气体通入澄清石灰水中,可以观察到澄清石灰水变浑浊;
得出的结论是污渍爆炸盐溶于水可以生成碳酸钠。

【题目】某班学生在老师指导下探究铁与水蒸气的反应,请帮助他完成下列实验报告。
(1)按图甲装好药品,连接装置(夹持仪器已略去)。其中A装置的作用是:_______
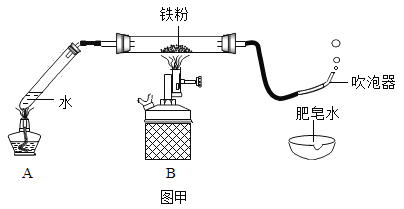
(2)加热一段时间后,灰色铁粉逐渐变黑,吹泡器连续吹出气泡,且气泡向上飞起;用燃着的木条靠近气泡,能产生爆鸣。
(3)同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
(查阅资料)铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色;铁的三种氧化物都不与硫酸铜溶液反应。
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
倒出玻璃管中黑色固体,平铺于白纸上 | 黑色固体不变色 | 黑色固体中一定没 有_____(填物质名称) |
取上述黑色固体少许,装入试管,加入足量硫酸铜溶液 | _____ ,有红色固体出现 | 黑色固体中一定 含有_____。 |