题目内容
【题目】溶液在日常生活、工农业生产和科学研究中具有广泛用途。
(1)KNO3属于复合肥,所含的营养元素有____________,溶质质量分数为3%的KNO3,溶液常用作无主栽培的营养液,配制100g该营养液需要的溶质是________,其质量为____g,配制时常用玻璃棒搅拌,目的是___________________。
(2)某KNO3固体(混有少量NaCl),要用它配制上述营养液,需在配制前进行提纯(图22为溶解度曲线),60°C时,KNO3的溶解度为____________g,将该固体溶于水配制为接近饱和的溶液,可采用降温结晶的方法提纯KNO3,其理由是________。
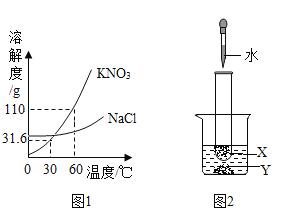
(3)探究温度对溶解度的影响,如图23所示。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2,烧杯中盛放20℃Y的饱和溶液(有少量Y的固体剩余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的组合_____________。
【答案】K、N 硝酸钾 3 加快溶解速率 110 硝酸钾的溶解度受温度的影响大,随温度降低其溶解度急剧减小,而氯化钠的溶解度受温度影响较小,故降温时硝酸钾晶体能析出 NH4NO3、Ca(OH)2或NaOH、KNO3
【解析】
(1)KNO3属于复合肥,所含的营养元素有钾元素和氮元素;溶质质量分数为3%的KNO3溶液常用作无土栽培的营养液,配制100g该营养液需要的溶质是硝酸钾;溶质质量=溶液质量×溶质质量分数,即溶质质量=100g×3%=3g;配制时常用玻璃棒搅拌,目的是:加快溶解速率;
(2)根据题目信息和溶解度曲线可知:60℃时,KNO3的溶解度为110g;将该固体溶于水配制为接近饱和的溶液,可采用降温结晶的方法提纯KNO3,其理由是:硝酸钾的溶解度受温度的影响大,随温度降低其溶解度急剧减小,而氯化钠的溶解度受温度影响较小,故降温时硝酸钾析出;
(3)如图2中,固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2,烧杯中盛放20℃Y的饱和溶液(有少量Y的固体剩余),往试管中滴入适量水,烧杯中固体逐渐消失,可以利用硝酸铵溶于水温度降低和氢氧化钙的溶解度随温度降低而增大;还可以利用氢氧化钠溶于水温度升高和硝酸甲的溶解度随温度升高而增大;则X与Y可能的组合:NH4NO3、Ca(OH)2;或NaOH、KNO3。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案【题目】某白色固体由BaSO4、BaCO3、NaCO3、Ba(OH)2中的三种物质组成。为确定其成分,某同学设计并完成如下实验,请把表格中的内容补充完整。(已知:BaSO4不溶于稀盐酸)

序号 | Ⅰ | Ⅱ | Ⅲ |
操作 |
|
| 先加入酚酞溶液再加入(3)_____
|
现象 | 有气泡产生,固体有剩余 | 有气泡产生 | 产生白色沉淀,溶液最终显(4)_____色 |
结论或解释 | 原白色固体中含有(1)_____ | 原白色固体中含有Na2CO3;生成气体的化学方程式为(2)_____ | 原白色固体中含有BaCO3 |