题目内容
【题目】草酸亚铁晶体(FeC2O4nH2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,某化学兴趣小组设计利用废弃铁锈合成草酸亚铁晶体并检验其热分解的产物及探究它的组成。
(一)制备草酸亚铁晶体(FeC2O4·nH2O)
资料1:FeSO4的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 | 59.8 |
资料2:草酸亚铁难溶于水,在酸性条件下稳定存在。
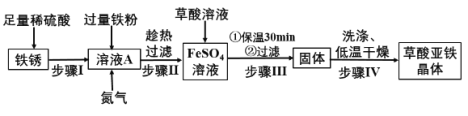
(制备流程)
(1)在实验室进行“过滤”操作时,需要的玻璃仪器有烧杯、漏斗和______,其作用是___
(2)步骤Ⅱ中趁热过滤的目的是______。
(3)草酸(H2C2O4)溶液加入FeSO4溶液中发生了复分解反应,请写出该反应的化学方程式为______。
(4)步骤Ⅲ中保温反应30min的目的是______。
(二)检验草酸亚铁晶体(FeC2O4·nH2O)热分解的产物及探究n的值
(实验装置)
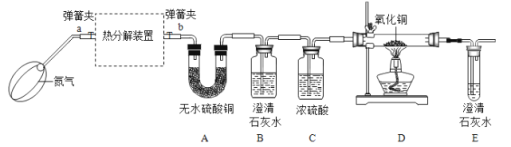
资料3:FeC2O4·nH2O加热至300℃完全失去结晶水;继续加热至400℃,剩余固体受热分解产生铁的氧化物、CO2和CO。
(实验分析)
(5)打开弹簧夹a、 b,先鼓入一段时间的氮气,然后再关闭a,加热分解装置的原因是______。
(6)若通过E装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解产生CO,则需在B和C装置之间增加盛有______(填试剂名称)的洗气瓶。
(7)装置D硬质玻璃管中出现的现象是______。
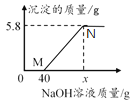
(8)取7.20gFeC2O4·nH2O,按上述实验步骤进行实验,测得热分解装置中固体质量随温度变化曲线如图所示:
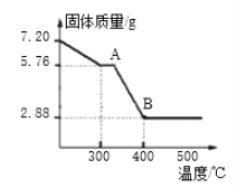
①FeC2O4·nH2O中n的值为______。(写出计算过程)
②若草酸亚铁晶体中混有杂质(杂质不参加反应),会导致测得的n的值______(选填“偏大”、“偏小”、“不变”)。/p>
③写出曲线中A至B发生反应的化学方程式______。
【答案】玻璃棒 引流 防止温度过低FeSO4晶体析出,造成损失 H2C2O4+FeSO4=FeC2O4↓+H2SO4 使反应物完全反应,得到更多产品使反应物完全反应,得到更多产品 排尽装置内的空气,防止空气中的水和二氧化碳干扰实验 氢氧化钠溶液 黑色固体变红 2 偏小 FeC2O4![]() FeO+CO↑+CO2↑
FeO+CO↑+CO2↑
【解析】
草酸亚铁晶体(FeC2O4nH2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,草酸亚铁难溶于水,在酸性条件下稳定存在,FeC2O4·nH2O加热至300℃完全失去结晶水,继续加热至400℃,剩余固体受热分解产生铁的氧化物、CO2和CO。
(1)在实验室进行“过滤”操作时,需要的玻璃仪器有烧杯、漏斗和玻璃棒,其作用是引流。
(2)FeSO4的溶解度随温度的升高而增大,温度降低会有晶体析出,步骤Ⅱ中趁热过滤的目的是防止温度过低FeSO4晶体析出,造成损失。
(3)草酸(H2C2O4)溶液加入FeSO4溶液中发生了复分解反应生成草酸亚铁沉淀和硫酸,反应的化学方程式为H2C2O4+FeSO4=FeC2O4↓+H2SO4。
(4)步骤Ⅲ中保温反应30min的目的是使反应物完全反应,得到更多产品使反应物完全反应,得到更多产品。
(5)打开弹簧夹a、 b,先鼓入一段时间的氮气,然后再关闭a,加热分解装置的原因是排尽装置内的空气,防止空气中的水和二氧化碳干扰实验排尽装置内的空气。
(6)若通过E装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解产生CO,则需在B和C装置之间增加盛有氢氧化钠溶液的洗气瓶,除去草酸亚铁晶体热分解产生的二氧化碳。
(7)装置D硬质玻璃管是氧化铜和一氧化碳反应生成铜和二氧化碳,出现的现象是黑色固体变红。
(8)①水的质量为![]()
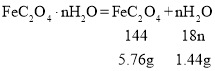
![]()
![]()
②若草酸亚铁晶体中混有杂质(杂质不参加反应),会导致测得的n的值偏小。
③曲线中A至B发生反应是草酸亚铁加热分解生成氧化亚铁和一氧化碳和二氧化碳,化学方程式为FeC2O4![]() FeO+CO↑+CO2↑。
FeO+CO↑+CO2↑。

【题目】水和溶液对于人类的生产和生命活动有重大的意义。
(1)能说明水是由氢元素和氧元素组成的实验是_____(填序号)。
A 水的净化 B 通电分解水 C 氢气在氧气中燃烧
(2)下表是三种物质在不同温度时的溶解度,根据表中信息回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度 |
|
|
|
|
|
|
| 119 | 190 | 286 | 421 | 630 | |
|
|
|
|
|
| |
①20℃时,将![]() 加入到
加入到![]() 水中充分搅拌后,所得溶液的质量为_____
水中充分搅拌后,所得溶液的质量为_____![]() 。
。
②40℃时,要使接近饱和的![]() 溶液变为饱和溶液,下列方法中一定能达到目的的是_____(填序号)。
溶液变为饱和溶液,下列方法中一定能达到目的的是_____(填序号)。
A 升高温度 B .加溶质![]() C .加水 D 恒温蒸发水
C .加水 D 恒温蒸发水
③60℃时,分别用![]() 、
、![]() 制成饱和溶液,需要水的质量
制成饱和溶液,需要水的质量![]() _____
_____![]() (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
④80℃时,向![]() 饱和溶液和
饱和溶液和![]() 饱和溶液中分别加入等量(少量)的
饱和溶液中分别加入等量(少量)的![]() 固体,在溶解过程中由饱和溶液变为不饱和溶液的是_____(填溶质的化学式)。
固体,在溶解过程中由饱和溶液变为不饱和溶液的是_____(填溶质的化学式)。
⑤某![]() 晶体中有少量
晶体中有少量![]() 和
和![]() 杂质,要得到纯净
杂质,要得到纯净![]() 的方法是:在80℃,向其中逐渐加水至全部溶解,然后_____、过滤、洗涤、干燥后得到
的方法是:在80℃,向其中逐渐加水至全部溶解,然后_____、过滤、洗涤、干燥后得到![]() 晶体。
晶体。
(3)实验室模拟工业粗盐精制的过程如下图所示。粗盐除含![]() 外,还含有少量
外,还含有少量![]() 、
、![]() 、
、![]() 和泥沙等杂质。
和泥沙等杂质。
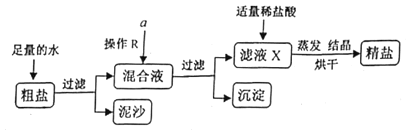
提供的试剂:![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液、饱和
溶液、饱和![]() 溶液。
溶液。
①过滤时使用玻璃棒的作用是_____。
②欲除去混合液中的杂质,从提供的试剂中选出![]() 所代表的除杂试剂,按滴加顺序依次为:过量的_____溶液、过量的
所代表的除杂试剂,按滴加顺序依次为:过量的_____溶液、过量的![]() 溶液、过量的
溶液、过量的![]() 溶液。
溶液。
③滤液![]() 中加入适量盐酸的目的是_____。
中加入适量盐酸的目的是_____。
④为充分反应得到较纯净的食盐,操作![]() 的具体方法是____。
的具体方法是____。