��Ŀ����
����Ŀ�����ۡ�8.12���ش���ֱ�ը�¹ʣ�����Ϊ�ⷿ�ڴ�ŵ�����立ֽ⣬��������ˮ��Ӧ�����ߵ��������϶�����ģ�
��֪��2NH4NO3 ![]() 2X��+O2��+4H2O����������ˮ���ҷ������������������ƣ�ͬʱ�ͷų��������ȣ�
2X��+O2��+4H2O����������ˮ���ҷ������������������ƣ�ͬʱ�ͷų��������ȣ�
��1��X�Ļ�ѧʽΪ��
��2�������ƺ�ˮ��Ӧ�Ļ�ѧ����ʽ��
��3������ը��ԭ�������û�ѧ����ʽ��ʾ����
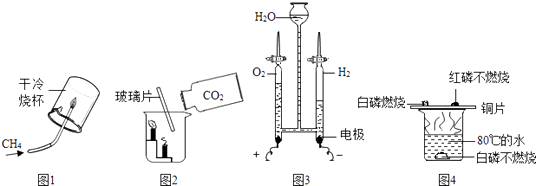
��4����������淋�����˵����ȷ������
A.������е�Ԫ�صĻ��ϼ�Ϊ+1��
B.�����Ӧ���´��
C.������к��������ӣ�������ɱ�ը��
���𰸡�
��1��N2
��2��2Na+2H2O=2NaOH+H2��
��3��2H2+O2 ![]() 2H2O
2H2O
��4��B
���������⣺��1�����������غ㶨�ɺͻ�ѧ����ʽ��֪��X�Ļ�ѧʽ�к��е�Ԫ�ص�ԭ�Ӹ���Ϊ��4��2=2��������Ԫ�ص�ԭ�Ӹ���Ϊ����8��8��=0��������Ԫ�ص�ԭ�Ӹ���Ϊ��6��2��4=0����X�Ļ�ѧʽΪ��N2�����N2����2������ˮ��Ӧ�����������ƺ���������ѧ����ʽΪ��2Na+2H2O=2NaOH+H2�������2Na+2H2O=2NaOH+H2������3������ը��ԭ���������������Ļ�����ȼ���£�����ȼ��������ˮ����ѧ����ʽ��2H2+O2 ![]() 2H2O�����2H2+O2
2H2O�����2H2+O2 ![]() 2H2O����4��A��������У�笠��е�Ԫ�صĻ��ϼ�Ϊ��3�ۣ��ʴ���
2H2O����4��A��������У�笠��е�Ԫ�صĻ��ϼ�Ϊ��3�ۣ��ʴ���
B������������ֽ⣬��Ӧ���´��棻��ȷ��
C��������в����������ӣ�����
��B��
�����㾫�������������غ㶨�ɼ���Ӧ�ú���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�ǽ����ĸ�������Ҫ֪���������غ㶨��ֻ�����ڻ�ѧ�仯���������������仯���ڲ��μӷ�Ӧ����������������������������������ܼ��롰�ܺ͡��У���Ҫ���ǿ����е������Ƿ�μӷ�Ӧ�����ʣ������壩������©��ע�⣺a����ƽ b������ c�����ţ�

 53���ò�ϵ�д�
53���ò�ϵ�д�����Ŀ����a��b��c��d�������ʷ���һ���ܱ������У���һ�������·�Ӧ��ʱ���ø����ʵ����������ʾ��������˵���д�����ǣ� ��
���� | a | b | c | d |
��Ӧǰ����/g | 6.4 | 3.2 | 4.0 | 0.5 |
��Ӧ������/g | ���� | 2.4 | 7.2 | 0.5 |
A.�÷�Ӧ���ڻ��Ϸ�Ӧ
B.D�����Ǵ�����Ҳ����������
C.�μӷ�Ӧ��a��b��������Ϊ2��1
D.��a��b����Է�������֮��Ϊ2��1�����仯ѧ������֮��Ϊ3��2