题目内容
过氧化钠(Na2O2)是一种淡黄色固体,常温下能与水和二氧化碳发生化学反应.
某学校两个实验小组的同学为探究其与二氧化碳的反应,用如图所示的装置进行实验.一段时间后,将带余烬的木条插入试管D中,木条复燃.

请回答下列问题:
(1)B装置的作用
(2)第2小组同学认为Na2O2与CO2反应除生成Na2CO3和O2外,还有可能生成NaHCO3.你认为呢?简述理由
(3)装置D的作用是
为了探究反应后试管D的溶液中是否有NaOH剩余,有同学设计实验方案,请帮助其完成下列实验报告.
某学校两个实验小组的同学为探究其与二氧化碳的反应,用如图所示的装置进行实验.一段时间后,将带余烬的木条插入试管D中,木条复燃.

请回答下列问题:
(1)B装置的作用
除去水分,防止过氧化钠与水反应
除去水分,防止过氧化钠与水反应
.(2)第2小组同学认为Na2O2与CO2反应除生成Na2CO3和O2外,还有可能生成NaHCO3.你认为呢?简述理由
不能;反应物中不含H元素
不能;反应物中不含H元素
.(3)装置D的作用是
吸收多余的二氧化碳(防止二氧化碳对检验氧气产生干扰)
吸收多余的二氧化碳(防止二氧化碳对检验氧气产生干扰)
.所发生的化学反应方程式:2NaOH+CO2═Na2CO3+H2O
2NaOH+CO2═Na2CO3+H2O
.为了探究反应后试管D的溶液中是否有NaOH剩余,有同学设计实验方案,请帮助其完成下列实验报告.
| 实验方案 | 实验现象 | 有关化学方程式 | 实验结论 |
| ①取样,先向溶液中滴加过量的 CaCl2或BaCl2或Ca(NO3)2或Ba(NO3)2 CaCl2或BaCl2或Ca(NO3)2或Ba(NO3)2 溶液; |
产生白色沉淀 | CaCl2+Na2CO3═CaCO3↓+2NaCl CaCl2+Na2CO3═CaCO3↓+2NaCl |
D溶液中有NaOH剩余. |
| ②静置,取上层清液,滴加 FeCl3或Fe(NO3)3 FeCl3或Fe(NO3)3 溶液. |
产生红褐色沉淀 | 3NaOH+FeCl3═Fe(OH)3↓+3NaCl 3NaOH+FeCl3═Fe(OH)3↓+3NaCl |
分析:(1)浓硫酸具有吸水性;过氧化钠能与水反应.
(2)根据质量守恒定律可知:化学反应前后元素种类不变.
(3)二氧化碳能与氢氧化钠溶液反应,从而除去生成的氧气中剩余的二氧化碳.
试管D中有生成的碳酸钠,探究氢氧化钠是否有剩余时,应先除去碳酸钠,并且不能产生新的氢氧化钠,以免影响探究结果.
氢氧化钠溶液能与氯化铁溶液反应生成红褐色的氢氧化铁沉淀,从而能判断氢氧化钠是否存在.
(2)根据质量守恒定律可知:化学反应前后元素种类不变.
(3)二氧化碳能与氢氧化钠溶液反应,从而除去生成的氧气中剩余的二氧化碳.
试管D中有生成的碳酸钠,探究氢氧化钠是否有剩余时,应先除去碳酸钠,并且不能产生新的氢氧化钠,以免影响探究结果.
氢氧化钠溶液能与氯化铁溶液反应生成红褐色的氢氧化铁沉淀,从而能判断氢氧化钠是否存在.
解答:解:(1)B装置中的浓硫酸具有吸水性,能够除去水分,防止过氧化钠与水反应.
(2)根据质量守恒定律可知:化学反应前后元素种类不变.由于反应物中没有氢元素,所以生成物中不可能含有氢元素,因此不能生成碳酸氢钠.
(3)二氧化碳能与氢氧化钠溶液反应,从而除去生成的氧气中剩余的二氧化碳,防止二氧化碳对检验氧气产生干扰.氯化钙(或氯化钡、硝酸钙、硫酸钡)能与碳酸钠反应生成碳酸钙(或碳酸钡)沉淀和氯化钠(或硝酸钠),从而除去碳酸钠,以免影响探究结果.该反应的化学方程式为(以氯化钙为例):CaCl2+Na2CO3=CaCO3↓+2NaCl.
氢氧化钠溶液能与氯化铁溶液反应生成红褐色的氢氧化铁沉淀和氯化钠.该反应的化学方程式为:3NaOH+FeCl3═Fe(OH)3↓+3NaCl.若有红褐色沉淀生成,说明试管D的溶液中氢氧化钠有剩余.
故答案为:
(1)除去水分,防止过氧化钠水反应;
(2)不能;反应物中不含H元素.
(4)吸收多余的二氧化碳(防止二氧化碳对检验氧气产生干扰);
(2)根据质量守恒定律可知:化学反应前后元素种类不变.由于反应物中没有氢元素,所以生成物中不可能含有氢元素,因此不能生成碳酸氢钠.
(3)二氧化碳能与氢氧化钠溶液反应,从而除去生成的氧气中剩余的二氧化碳,防止二氧化碳对检验氧气产生干扰.氯化钙(或氯化钡、硝酸钙、硫酸钡)能与碳酸钠反应生成碳酸钙(或碳酸钡)沉淀和氯化钠(或硝酸钠),从而除去碳酸钠,以免影响探究结果.该反应的化学方程式为(以氯化钙为例):CaCl2+Na2CO3=CaCO3↓+2NaCl.
氢氧化钠溶液能与氯化铁溶液反应生成红褐色的氢氧化铁沉淀和氯化钠.该反应的化学方程式为:3NaOH+FeCl3═Fe(OH)3↓+3NaCl.若有红褐色沉淀生成,说明试管D的溶液中氢氧化钠有剩余.
故答案为:
(1)除去水分,防止过氧化钠水反应;
(2)不能;反应物中不含H元素.
(4)吸收多余的二氧化碳(防止二氧化碳对检验氧气产生干扰);
| 实验方案 | 实验现象 | 有关化学方程式 | 实验结论 |
| ①CaCl2或BaCl2或Ca(NO3)2或Ba(NO3)2 | CaCl2+Na2CO3═CaCO3↓+2NaCl | ||
| ②FeCl3或Fe(NO3)3 | 3NaOH+FeCl3═Fe(OH)3↓+3NaCl |
点评:本题主要考查二氧化碳的制取和干燥、氧气的制取和除杂、质量守恒定律的应用、物质的探究等问题,难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
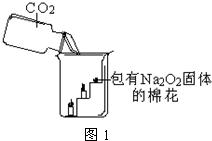


 23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
