题目内容
为了测定某石灰石样品中碳酸钙的质量分数(杂质不参加反应)某学习小组取来了一些石灰石样品,并取稀盐酸200g平均分成四份进行了四次实验,结果如表:
(1)第4次实验中m的值为
(2)求该石灰石样品中碳酸钙的质量分数.
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入石灰石样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
(2)求该石灰石样品中碳酸钙的质量分数.
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)观察并对比表格中的数据可知:第2次实验中的数据均为第一次实验的两倍,而第3次少,说明此时盐酸已完全反应,故3、4次实验中碳酸钙有剩余;3、4次实验中碳酸钙有剩余,且生成二氧化碳的质量相等,即m=4.4;
(2)根据矿石中碳酸钙完全反应的那次产生二氧化碳的质量计算出碳酸钙的质量,用碳酸钙的质量除以矿石的质量即可.
(2)根据矿石中碳酸钙完全反应的那次产生二氧化碳的质量计算出碳酸钙的质量,用碳酸钙的质量除以矿石的质量即可.
解答:解:(1)由表格中的数据可知,第3次反应已是完全反应,故第3、4次反应中的碳酸钙的质量有剩余;因为第3次反应已是完全反应,不再有气体产生,故第四次反应生成的气体质量的第三次的一样多,即m=4.4;故填:4.4;
(2)由图可知5g样品完全反应产生1.76g 二氧化碳,设5克石灰石中碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 1.76g
=
x=4g
石灰石中碳酸钙的质量分数=
×100%=80%
答:石灰石中碳酸钙的质量分数为80%.
(2)由图可知5g样品完全反应产生1.76g 二氧化碳,设5克石灰石中碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 1.76g
| 100 |
| x |
| 44 |
| 1.76g |
x=4g
石灰石中碳酸钙的质量分数=
| 4g |
| 5g |
答:石灰石中碳酸钙的质量分数为80%.
点评:通过回答本题知道了通过图表数据分析哪次完全反应,哪次有剩余的方法,并进一步巩固了计算题的解题步骤,解答本题的关键是分析出第三次盐酸已经被反应完了,再进一步进行推证即可.

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
下列物质中前者属于纯净物,后者属于混合物的是( )
| A、糖水、水 |
| B、空气、酱油 |
| C、冰水混合物、盐水 |
| D、氮气、氦气 |
如图所示下列实验设计,能达到实验目的是( )
A、 此图装置探究空气中氧气的含量 |
B、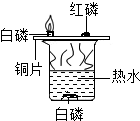 此图装置验证可燃物燃烧的两个条件 |
C、 此图装置检验二氧化碳 |
D、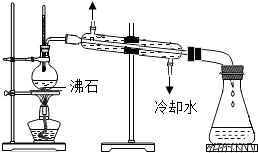 此图装置制取蒸馏水 |
下列对课本中相关实验的分析不正确的是( )
| A、电解水实验能说明水由氢、氧两种元素组成 |
| B、氢氧化钠与硫酸铜溶液反应前后质量的测定实验能说明化学反应遵循质量守恒定律 |
| C、从斜面上滚动下来的小球推动木块走的距离越远,说明木块的动能越大 |
| D、在探究电路的电流规律实验时,开关断开,发现两灯都灭,则可能是并联电路 |
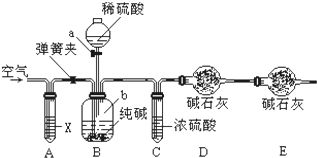 某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:
某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下: