��Ŀ����
����Ŀ��ij�о���ѧϰС������˲ⶨ���Na2CO3����Ʒ������ֻ��NaCl���ʣ���Na2CO3����������ʵ�鷽��������������ǵ�̽�������ش��������⣺��������ԭװ���ڿ�����Ӱ����
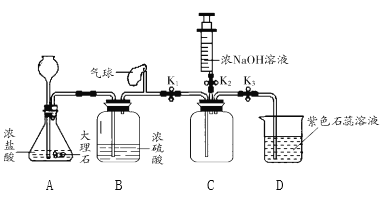
����A��ͬѧ�������ͼ1��ʵ��װ�á�

��1��ʵ��ʱ����װҩƷǰ����װ����ͼ��������_________��
��2��װ���ҵ�������_________��
��3��װ�ö���������_________��������ĸ��
A������Na2CO3������Һ��Ӧ����CO2
B����ֹ�����ж�����̼��ˮ��������װ�ñ���
C�����������̼
��4��ʵ��������μ�����Һ���ٶȹ��죬�ᵼ�²����Ʒ��̼���Ƶ���������____������ƫ��������ƫС��������Ӱ��������
��5��B��ͬѧ��ΪA��ͬѧ�ķ����������⣬��ʹ�����淶���ⶨ���Ҳ��ƫ�ͣ�������_________��Ӧ�ý�װ�ü���˫�����������������������ڼ����������ͼ2װ�ã�ʵ�������ͨ��һ��ʱ�������Ŀ����_________������NaOH��Һ��������________����û��ͼ2װ�ã�ֱ��ͨ���������ᵼ�²�ý��_________������ƫ��������ƫС��������Ӱ��������
��6������Ϊʵ��ʱ���������Һ�����_________������ϡ����������ϡ����������
����С��ͬѧ��ȡ��Ʒ11.0g�����ձ��У�������ʵ�鷽������ʵ�顣

��1����ҺY�к��е�������_________����д��ѧʽ����
��2��֤��CaCl2�ѹ����ķ�����_________����д��ĸ��ţ���Ȼ��۲������жϡ�
A����������ҺX�����ϲ���Һ�м����μ������Ȼ�����Һ
B��ȡ������ҺY���Թ��У��μ��Ȼ�����Һ
��3���������û��ϴ�Ӳ��������̼������������________������ƫ��������ƫС��������Ӱ��������
��4��ͨ�������ṩ�����ݼ������Ʒ��̼���Ƶ���������Ϊ_________����д��������̣����������0.1%��
���𰸡� ���װ�������� ��ȥCO2��ˮ�����������CO2�� B ƫС ��CO2��������ƿ�� ��������CO2ȫ�����뵽��װ���У�ʹ����ȫ������������Һ���� ��ȥͨ������е�CO2 ƫ�� ϡ���� CaCl2 ��NaCl A ƫ�� 96.4%
��������������1����ȡ����ʱ�����ȼ��װ�õ������ԣ�
��2��Ũ��������ˮ�ԣ���ȥCO2��ˮ����������CO2��
��3�����еļ�ʯ�ҷ�ֹ�����ж�����̼��ˮ��������װ�ñ��У�Ӱ����㣻
��4��ʵ���еμ�ϡ������ٶȹ��죬����������������������̼������ȫ������������Һ���գ����²����Ʒ��̼���Ƶ���������ƫ�ͣ�
��5������A��ͬѧ�ķ�������Ӧ��ȫ����CO2��������ƿ�ڣ����ܱ�װ�ñ���ҩƷ���գ���ɲ����Ʒ��̼���Ƶ���������ƫ�ͣ���װ�ü���˫��������������������������ͼ2װ�ã�ʵ�������ͨ��һ��ʱ�������Ŀ���ǽ�������CO2ȫ�����뵽��װ���У�ʹ����ȫ������������Һ���գ�����NaOH��Һ�����������տ����е�CO2��ֱ��ͨ�������ʹ�ÿ����еĶ�����̼Ҳ��װ�ñ���ҩƷ���գ���ᵼ�²�ý��ƫ��
��6������������лӷ��ԣ��ᷢ�����Ȼ������壬��װ�ñ���ҩƷ���գ���ᵼ�²�ý��ƫ��������ϡ���
������1��������Ʒֻ��NaCl���ʣ�̼�������Ȼ��Ʒ�Ӧ����̼��ƺ��Ȼ��ƣ������Ȼ�����Һ���������Է�Ӧ������Һ�к���CaCl2 ��NaCl��
��2��CaCl2�ѹ���������Һ�в���̼���ƣ���������ҺX�����ϲ���Һ�м����μ������Ȼ�����Һ�����������ɫ������˵��CaCl2�ѹ�����
��3����Ϊ�ڳ�������Ŀ����������Ȼ��ƣ����Գ���ϴ�ӵ�Ŀ���ǣ���ȥ��������Ŀ��������ʣ�����ϴ�ӣ������Ȼ��Ƶ��������������������������Ʒ��������̼���ƫ����̼���Ƶ���������ƫ��
��4������Ʒ��̼���Ƶ�������X
CaCl2+Na2CO3�TCaCO3��+2NaCl
106 100
X 10.0g
![]()
X=10.6g
��Ʒ��̼���Ƶ���������Ϊ![]() ��100%=93.4%��
��100%=93.4%��
����Ʒ��̼���Ƶ���������Ϊ93.4%��

 Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д� ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�