题目内容
 根据如图A、B、C三种固体的溶解度曲线回答:
根据如图A、B、C三种固体的溶解度曲线回答:
(1)20℃时,欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是A________B:(填写“>”、“<”或“=”)
(2)要在不改变溶质的质量分数的前提下使50℃时C的饱和溶液成为不饱和溶液,可采用的方法是________.
(3)将50℃时三种物质的饱和溶液分别都降温到20℃,此时溶液中溶质的质量分数从大到小是________.
(4)甲、乙两烧杯中分别装有50℃的100克和200克A的饱和溶液,若将两份溶液都降低到20℃,析出晶体质量的关系是甲________乙(填写“>”、“<”或“=”),若将两份溶液都恒温蒸发10克水,析出晶体质量的关系是甲________乙.
(5)欲从混有少量A的B物质的饱和溶液中得到纯净的B晶体,应该采用的方法是________.
解:(1)20℃时,B物质的溶解度大于A物质的溶解度,根据溶解度的定义可以知道欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是A>B;
(2)C的溶解度随温度的升高而减小,所以要在不改变溶质的质量分数的前提下使50℃时C的饱和溶液成为不饱和溶液,可采用的方法是降低温度;
(3)将50℃时三种物质的饱和溶液分别都降温到20℃,C的溶解度随温度的升高而减小,所以降低温度对C的溶质的质量分数没有影响,分析20℃时的溶解度可以知道,A的溶解度小于B的溶解度,但是大于50℃时C的溶解度,所以若将50℃时三种物质的饱和溶液分别都降温到20℃,此时溶液中溶质的质量分数从大到小是B>A>C;
(4)50℃时200克A的饱和溶液比100克A的饱和溶液含有的溶质多,所以若将两份溶液都降低到20℃,析出晶体质量的关系是甲<乙,若将两份溶液都恒温蒸发10克水,由于是同一种物质,所以析出的晶体析出晶体质量的关系是甲=乙.
(5)A的溶解度受温度变化影响大,而B物质的溶解度受温度变化影响较小,所以欲从混有少量A的B物质的饱和溶液中得到纯净的B晶体,应该采用的方法是冷却热饱和溶液的方法.
故答案为:(1)>;
(2)降低;
(3)B>A>C;
(4)<;=;
(5)冷却热饱和溶液.
分析:固体溶解度曲线所能表示的意义:①根据已知的温度可以查出有关物质的溶解度;②根据物质的溶解度也可以查出它所对应的温度;③可以判断或比较相同温度下,不同物质溶解度的大小(或饱和溶液中溶质的质量分数的大小);④根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶);并且,还可以判断或比较析出晶体的质量大小,即曲线越陡,析出的晶体就越多;⑤两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的.
可以据此以上几点来完成解答.
点评:解答这类题目时,首先,要熟记和理解固体溶解度曲线及其使用,固体溶解度的概念和意义,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法,以及物质的溶解和结晶的方法等相关知识;然后,根据所给的问题情景或结合所学的相关知识和技能,按照题目的要求,认真地进行选择或解答即可.
(2)C的溶解度随温度的升高而减小,所以要在不改变溶质的质量分数的前提下使50℃时C的饱和溶液成为不饱和溶液,可采用的方法是降低温度;
(3)将50℃时三种物质的饱和溶液分别都降温到20℃,C的溶解度随温度的升高而减小,所以降低温度对C的溶质的质量分数没有影响,分析20℃时的溶解度可以知道,A的溶解度小于B的溶解度,但是大于50℃时C的溶解度,所以若将50℃时三种物质的饱和溶液分别都降温到20℃,此时溶液中溶质的质量分数从大到小是B>A>C;
(4)50℃时200克A的饱和溶液比100克A的饱和溶液含有的溶质多,所以若将两份溶液都降低到20℃,析出晶体质量的关系是甲<乙,若将两份溶液都恒温蒸发10克水,由于是同一种物质,所以析出的晶体析出晶体质量的关系是甲=乙.
(5)A的溶解度受温度变化影响大,而B物质的溶解度受温度变化影响较小,所以欲从混有少量A的B物质的饱和溶液中得到纯净的B晶体,应该采用的方法是冷却热饱和溶液的方法.
故答案为:(1)>;
(2)降低;
(3)B>A>C;
(4)<;=;
(5)冷却热饱和溶液.
分析:固体溶解度曲线所能表示的意义:①根据已知的温度可以查出有关物质的溶解度;②根据物质的溶解度也可以查出它所对应的温度;③可以判断或比较相同温度下,不同物质溶解度的大小(或饱和溶液中溶质的质量分数的大小);④根据溶解度曲线,选择分离、提纯某些可溶性混合物的方法(即选用蒸发结晶还是降温结晶);并且,还可以判断或比较析出晶体的质量大小,即曲线越陡,析出的晶体就越多;⑤两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的;并且,此时两种物质饱和溶液的溶质质量分数也相同的.
可以据此以上几点来完成解答.
点评:解答这类题目时,首先,要熟记和理解固体溶解度曲线及其使用,固体溶解度的概念和意义,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法,以及物质的溶解和结晶的方法等相关知识;然后,根据所给的问题情景或结合所学的相关知识和技能,按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
相关题目
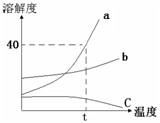 23、根据如图a、b、c三种物质的溶解度曲线,回答下列问题.
23、根据如图a、b、c三种物质的溶解度曲线,回答下列问题.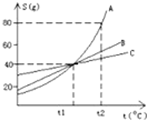
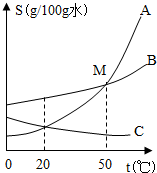 (2012?虹口区二模)根据如图A、B、C三种固体的溶解度曲线回答:
(2012?虹口区二模)根据如图A、B、C三种固体的溶解度曲线回答: 根据如图A、B、C三种固体的溶解度曲线回答:
根据如图A、B、C三种固体的溶解度曲线回答: 根据如图A、B、C三种固体物质的溶解度曲线,下列说法正确的是( )
根据如图A、B、C三种固体物质的溶解度曲线,下列说法正确的是( )