题目内容
【题目】实验操作考试时,晓楠误将氢氧化钠溶液当成酸滴加到金属铝中,结果发现溶液中有气泡产生!为了解该异常操作中产生的气体的成分,实验小组进行了以下探究:
【提出猜想】猜想:Ⅰ氧气;Ⅱ氢气;Ⅲ二氧化硫
同学们一致认为猜想Ⅲ是错误的,理由是_________________________________________;
【进行实验】
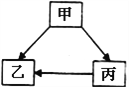
在进行实验之前,应当先_____________________,然后利用图甲所示的装置进行实验。

(1)反应一段时间后,将产生的气体通过管口a收集起来,发现该气体不能供给呼吸,则猜想Ⅰ错误。
(2)①用图乙所示的装置干燥从管口a导出来的气体时,应将管口a与b端管口连接,通入装有_____________的集气瓶中。
②反应一段时间,点燃得到的干燥气体,通过对现象的分析得出猜想Ⅱ正确。
【得出结论】
(1)通过查阅资料得知:铝、水和氢氧化钠反应会产生氢气和偏铝酸钠(NaAlO2),则该反应的化学方程式为:_________________________________________。
(2)铝是一种性质特殊的金属,它可以同时和酸、碱反应放出氢气。
【交流讨论】
有同学认为,晓楠的实验方案有欠缺:(1)她应该在点燃气体之前______________________;
(2)为了保证实验结果的可靠性,她应该_________________________________________。
【反思提升】
(1)_______________________________________________________________。
(2)实验过程中一定要注意安全。
【答案】 不符合质量守恒定律(或反应物中不含硫元素) 检查装置的气密性 浓硫酸 2Al + 2NaOH + 2H2O===2NaAlO2 + 3H2↑ 检验纯度 重复进行实验 面对实验中的异常现象应当利用所学知识继续探究(合理即可)
【解析】【提出猜想】根据质量守恒定律,化学反应前后元素的种类不变,反应前无碳元素,反应后也无硫元素,故猜想Ⅲ是错误的;
【进行实验】做有关气体的实验前一定先检查装置的气密性;浓硫酸有吸水性,可作干燥剂;
【得出结论】铝、水和氢氧化钠反应会产生氢气和偏铝酸钠(NaAlO2),化学方程式为:2Al + 2NaOH + 2H2O=2NaAlO2 + 3H2↑;
【交流讨论】(1)氢气具有可燃性,点燃时易发生爆炸,所以在点燃气体之前检验纯度;
(2)为了保证实验结果的可靠性,避免偶然性,应重复进行实验;
【反思提升】根据本题的探究,我们今后面对实验中的异常现象应当利用所学知识继续探究(合理即可)。

 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案【题目】一些食物的近似pH如下:
食物 | 葡萄汁 | 苹果汁 | 牛奶 | 玉米粥 | 鸡蛋清 |
pH | 3.5~4.5 | 2.9~3.3 | 6.3~6.6 | 7.0~8.0 | 7.6~8.0 |
下列说法不正确的是
A. 鸡蛋清显碱性 B. 苹果汁和葡萄汁显酸性
C. 葡萄汁比苹果汁的酸性强 D. 胃酸过多的人适宜吃玉米粥